какие противозачаточные можно принимать при эндометриозе
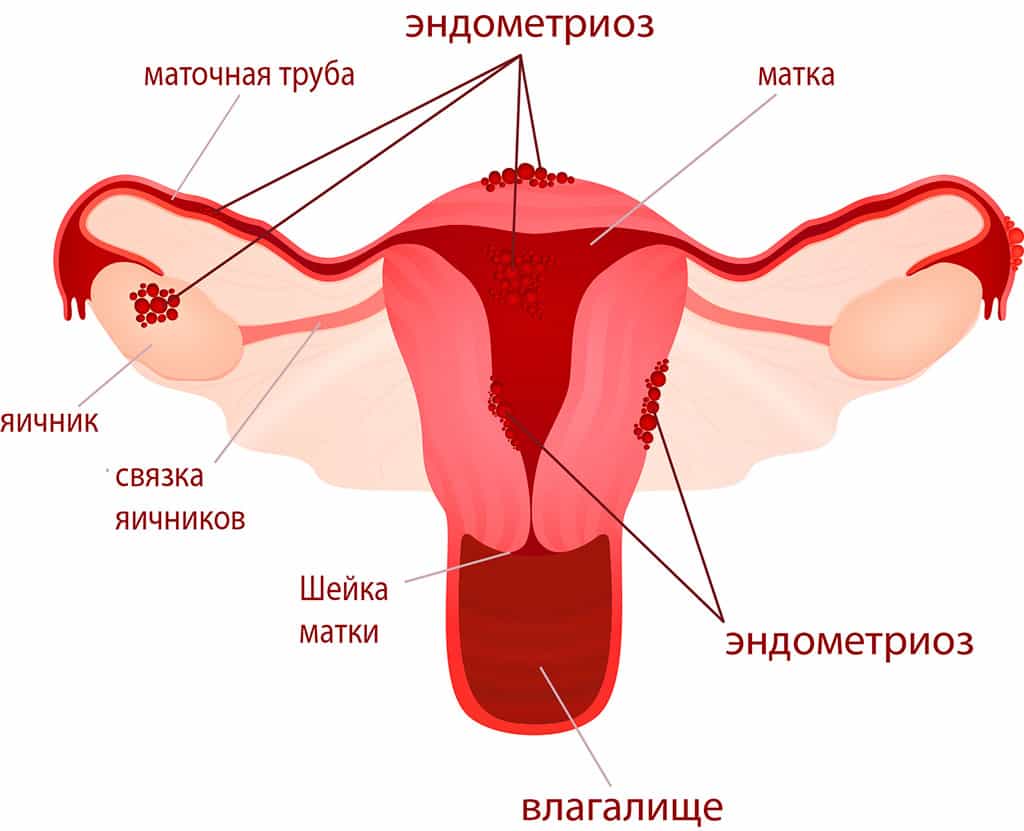
Эндометриоз
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Эндометриоз обнаруживается не только отделах репродуктивной системы, но и вне ее (брюшная стенка, мочевыделительная система, пищеварительный тракт, брюшина, легкие и пр.). Клинические проявления разнообразны и зависеть от расположения патологического процесса. Могут выражаться: болью, нарушениями менструального цикла (кровянистых выделений перед началом менструации, контактных кровянистых выделений).
Причины эндометриоза
Единой версии причин возникновения эндометриоза на сегодняшний день нет.
1 теория: «Ретроградная менструация или имплантационная теория»
У некоторых женщин имеется склонность к такой особенности как ретроградная менструация (когда мышечный слой матки сокращается в обратном направлении от шейки матки). В период месячных (регул) кровь с элементами эндометрия за счет перистальтических движений гладкомышечной мускулатуры матки заносится в брюшную полость и фаллопиевы трубы, где эндометрий имплантируется в ткани различных органов. В течение обычного менструального цикла внутренний слой матки (эндометрий) отделяется и выводится из полости матки, в то время как в других органах, пораженных эндометриозными очагами, происходят микрокровоизлияния и возникает асептическое воспаление. Вероятность появления эндометриоза может увеличиться от таких причин как: особенности строения маточных придатков, иммунные патологические процессы, аборты, операции на матке, кесарево сечение, оперативное лечение заболеваний шейки матки, наследственная предрасположенность.
Особенно высока роль наследственности при рассматриваемой патологии и предполагает весьма высокую возможность возникновения болезни у дочери, если её мать ранее перенесла такое заболевание. Зная о предрасположенности к данной патологии, женщина, соблюдая меры профилактики, может предотвратить возникновение болезни. Так, например, после оперативных вмешательств на органах репродуктивной системы женщине необходим систематический контроль состояния здоровья для предотвращения возможных осложнений.
2 теория: «Генные мутации»
3 теория: «Отклонения в функции клеточных ферментов и реакции рецепторов к гормонам»
Однако, последние две теории не получили повсеместной популяризации в связи с малой базой доказательности. Классификация эндометриоза разделяется по локализации.
Классификация эндометриоза
Генитальный. Из самого названия следует, что при течении болезни в этой форме эндометриозные очаги располагаются в тканях детородных органов пациентки.
Экстраперитонеальный (внебрюшинный) эндометриоз возникает в органах не покрытых брюшиной: в нижних частях половых органов, вульве, в шейке матки (ее влагалищном сегменте), позадивагинальной перегородке и пр. В мускульном слое матки может сформироваться внутренний эндометриоз (аденомиоз), при этом матка обретает шаровидную форму и достигает величины до 5-6 недели беременности.
Экстрагенитальный эндометриоз. При этой форме эндометриозные очаги находятся за пределами репродуктивной системы (пищеварительный тракт, дыхательная система, мочевыделительная система, послеоперационные рубцы).
При серьезных, осложненных случаях болезни эндометриоз бывает смешанный.
В зависимости от глубины и распространения очагов эндометриоза различают 4 степени:
В зависимости от цикличности регул эндометриозные очаги большей частью проявляются в преддверии месячных. Очаги имеют самую различную локализацию и обнаруживаются не только на поверхности органов, но и проявляют тенденцию к глубокой инвазии в ткани. При вовлечении яичников в процесс эндометриоза кисты сгруппированы и наполнены кровянистым содержимым. Исходя из размеров и глубины эндометриозных поражений, а также локализации образований, степень эндометриоза определяют по бальной системе.
Симптомы эндометриоза
Тазовая боль. Возникает у 16-24% пациенток. Может иметь как точечную, так и разлитую локализацию, возникает и усиливается в корреляции от менструального цикла, может быть и постоянной. Зачастую она вызвана с воспалением и спаечным процессом, развивающимися при поражении эндометриозом.
Постгеморрагическая анемия. У 25-40% пациенток из-за значительной хронической кровопотери во время менструаций может возникнуть состояние малокровия. Постепенно нарастает слабость, бледность или желтушность кожных и слизистых покровов, головокружение, утомляемость, сонливостью раздражительность и психической возбудимостью.
Бесплодие. Точно дать оценку тому, как и почему возникает бесплодие при поражении эндометриозом, ученые и врачи сегодня не в силах. Связывают это с процессами в придатках матки при эндометриозе, с перебоями в функционировании общего и местного иммунного статуса организма в целом, и как итог- сбои в овуляторных процессах. Не абсолютна, но достаточно высока при эндометриозе возможность не наступления беременности. Эндометриоз и сопутствующие ему процессы могут провоцировать самопроизвольные аборты, которые в свою очередь, кардинально и значительно сокращают шансы не только на наступление беременности, но и на нормальное её течение. Поэтому беременные с эндометриозом в анамнезе должны постоянно наблюдаться у врача.15- 56% пролеченных от эндометриоза пациенток беременеют в течение 6-12 месяцев.
Диагностика эндометриоза
С внедрением малоинвазивных методов диагностики и лечения (гистероскопии и лапароскопии) выявляемость эндометриоза значительно увеличилась.
В силу своей схожести протекания данного заболевания с другими, похожими по симптоматике, заболеваниями половых органов, на всех этапах постановки диагноза очень важное значение имеет дифференциальная диагностика. Врач тщательно собирает жалобы и анамнез, информацию о перенесенных заболеваниях, в том числе репродуктивной системы, хирургических операциях, наличии гинекологического и акушерского отягощённого анамнеза у родственников по женской линии.
Дальнейшее обследование включает в себя:
Комплекс всех методов позволяет выявить эндометриозные очаги до 96% случаев.
Заключительный диагноз можно поставить только в том случае, если произведено гистологическое исследование биоптата из очагов эндометриоза, взятых при проведении гистероскопии (лапароскопии).
Лечение эндометриоза
Очень важно в определении тактики терапии эндометриоза учитывать следующие факторы:
к какой возрастной категории относится пациентка,
количество беременностей, в том числе окончившихся родоразрешениями,
важно знать, как протекали роды и не было-ли в послеродовом периоде каких-либо осложнений,
учитывается тяжесть патологического процесса, его местонахождение, глубина, сопутствующие патологии, желание родить ребенка.
При терапии эндометриоза действия врача направлены не просто на устранение проявлений рассматриваемой болезни, но и её последствий (спаечные и кистозные образования, психоневрологические проявления, пр.).
Оперативное лечение эндометриоза
При средней и тяжелой стадиях эндометриоза рекомендуется прибегать к органосохраняющему хирургическому лечению с удалением очагов. Лечение всесторонне нацелено на резекцию гетеротопий в пораженных органокомплексах, резекцию эндометриоидных кист в яичниках, а также рассекание спаек. Как правило, оно применяется, если эффект от медикаментозного лечения отсутствует, имеются различные противопоказания, например непереносимость препаратов или их компонентов, при обнаружении эндометриоидных новообразований размером более 3-4 сантиметров, дисфункции мочевыделения, проблемах с желудочно-кишечным трактом. Зачастую оперативное лечение совмещают с лекарственным. Вмешательство осуществляют лапароскопическим или лапаротомным доступами.
Если у пациентки в возрасте после 40 лет активно прогрессирует заболевание и консервативно-хирургические мероприятия не дают должного эффекта, то прибегают к радикальному хирургическому удалению эндометриоза (экстирпация матки с придатками). Такие мероприятия применяются не часто и встречаются у 12% пациенток.
Основные принципы хирургического лечения эндометриоза с позиций доказательной медицины
Независимо от того, насколько далеко и глубоко распространился патологический процесс, лапароскопия является предпочтительным хирургическим доступом («золотой стандарт») при лечении эндометриоза. Она способствует лучшей визуализации очагов, благодаря их оптическому увеличению, минимальной травматизации тканей и более быстрой реабилитации пациенток, чем после лапаротомии. Лечебно-диагностическая лапароскопия с удалением эндометриозных новообразований обеспечивает значительное уменьшение интенсивности ассоциированных с эндометриозом болей.
Эндометриомы яичников у женщин с тазовой болью должны быть удалены хирургическим путем при лапароскопии.
Женщинам в детородном возрасте принципиально важно излечиться от эндометриоза яичников без риска рецидивирования с максимальным сохранением не поражённой ткани овоцитов. Для этого выполняют пункцию, дренирование кисты, алкоголизацию и уничтожение капсулы путем воздействия энергии различных видов. Однако, все эти методы не позволяют полностью удалить капсулу кисты, что может привести к рецидиву болезни.
У женщин, незаинтересованных в беременности эндометриозные очаги могут быть удалены лапароскопическим или комбинированным лапароскопически-влагалищным доступом, при необходимости в сочетании с одновременной резекцией пораженного участка стенки прямой кишки или в едином блоке с маткой.
Радикальным методом лечения аденомиоза можно считать лишь удаление матки (экстирпация матки). Данная операция, как правило, производится лапароскопическим путем. При выполнении операции по удалению матки очень важно удалить все видимые эндометриоидные очаги, при этом двухстороннее удаление яичников может способствовать более эффективному исчезновению боли и уменьшению вероятности рецидива заболевания.
С каждой пациенткой индивидуально должен обсуждаться вопрос об удалении яичников.
Консервативное лечение применяется, если эндометриоз имеет скрытое латентное течение, возраст пациентки до 45 лет, во время пременопаузы, и имеется потребность сохранения репродуктивной функции.
Гормонотерапия при лечении эндометриоза
Полная реконвалесценция при эндометриозе наступает только при его раннем выявлении и качественной последующей терапии.
Оценочными показателями выздоровления от эндометриоза являются: хорошее самочувствие, отсутствие жалоб на тазовые боли, непоявление рецидивов в течение 5 лет после терапии, восстановление или сохранение функции деторождения.
При современном уровне развитости хирургической гинекологии с обширным использованием органосохраняющих методов лечения, всего вышеперечисленного можно добиться у 60% женщин возрасте от 20 до 36 лет. Если пациентка была оказана помощь в виде радикальной операции, то заболевание не рецидивирует.
1. Эндометриоидные кисты яичников («шоколадные» кисты), заполненные старой менструальной кровью.
2. Кровоизлияния и рубцовые изменения.
Эти два осложнения с большой долей вероятности могут привести к состоянию бесплодия. Обширные и распространенные эндометриозные очаги оказывают давление на нервные стволы и окончания, что приводит к разнообразным неврологическим нарушениям. Редко встречается озлокачествление перерожденных очагов эндометриоза. По данным ученых, у женщин с эндометриозом риск развития онкологических перерождений на 50% выше среднестатистических.
Профилактика эндометриоза
Чем раньше при появлении первых симптомов эндометриоза женщина приходит на консультацию к гинекологу, тем выше шанс на полное избавление необходимости оперативного лечения. Попытки самостоятельной терапии или отсрочка обращения за помощью совершенно не оправданы: с очередным менструальным циклом появляются новые эндометриозные очаги, возникают кисты, усиливаются рубцовые и спаечные процессы, усугубляется состояние фаллопиевых труб.
Для профилактики эндометриоза, необходимо:
обследование девочек-подростков и женщин с жалобами на боли во время месячных;
курирование пациенток после абортов и других иных манипуляций на матке для ликвидации возможных последствий;
своевременная и полная элиминация острых и хронических патологий гениталий;
прием оральных гормональных контрацептивов.
Риск возникновения эндометриоза выше у курящих женщин в возрасте после 30-35 лет с коротким менструальным циклом, страдающих нарушениями метаболизма, ожирением, излишним весом; имеющих внутриматочные контрацептивы; с повышенным уровнем эстрогенов; страдающих иммунодепрессией; имеющих наследственную предрасположенность и перенесших операции на матке.
Какие противозачаточные можно принимать при эндометриозе
ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» Минобрнауки; ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России
Гормональные контрацептивы и эндометриоз: современный взгляд на проблему
Журнал: Проблемы репродукции. 2020;26(3): 39-45
Ярмолинская М.И., Адамян Л.В. Гормональные контрацептивы и эндометриоз: современный взгляд на проблему. Проблемы репродукции. 2020;26(3):39-45.
Yarmolinskaya MI, Adamyan LV. Hormonal contraceptives and endometriosis: modern view on the problem. Russian Journal of Human Reproduction. 2020;26(3):39-45.
https://doi.org/10.17116/repro20202603139
ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» Минобрнауки; ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России
В статье обобщены современные данные о применении у больных с генитальным эндометриозом гормональных контрацептивов: комбинированных эстроген-гестагенных препаратов, в том числе имеющих в своем составе эстрогены, биоидентичные натуральным; только прогестагенсодержащих контрацептивов, включая внутриматочную рилизинг-систему. Приведены доказательства эффективности и патогенетической обоснованности пролонгированных схем назначения микродозированных по дозе эстрогенного компонента препаратов, а также показания к выбору прогестинов с целью контрацепции. Авторами представлен алгоритм применения гормональных контрацептивов при тяжелом инфильтративном эндометриозе, а также при экстрагенитальной его локализации.
ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» Минобрнауки; ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России
Даты принятия в печать:
Накоплен многолетний мировой опыт применения комбинированных оральных контрацептивов (КОК) с целью лечения наружного генитального эндометриоза (НГЭ), создана доказательная база относительно профилактических и лечебных эффектов КОК. Вместе с тем специалисты продолжают обсуждать вопрос о применении эстроген-гестагенных препаратов у данной категории больных.
Согласно федеральным клиническим рекомендациям по ведению больных с эндометриозом [1], при наличии такого симптома, как дисменорея легкой или средней степени выраженности, возможно эмпирическое назначение комбинированных гормональных контрацептивов или прогестагенов. При выборе препарата для длительной терапии преимуществами КОК являются доказанная безопасность [2], надежная контрацепция, хороший контроль менструального цикла, купирование симптомов предменструального синдрома и, как следствие, улучшение психо-эмоционального состояния пациентки, что в свою очередь увеличивает приверженность к данному методу лечения [2].
На 13-м Всемирном конгрессе по эндометриозу (Ванкувер, 2017 г.) обобщены рекомендации мировых экспертов [3, 4], сформулирован тезис о целесообразности назначения КОК пациентке с НГЭ, не планирующей беременность и нуждающейся в контрацепции. Согласно рекомендациям Европейского общества репродукции человека и эмбриологии (European Society of Human Reproduction and Embryology, ESHRE) [5], Национального института здоровья и совершенствования медицинской помощи Великобритании (National Institute for Health and Care Excellence, NICE) [6], применение КОК в различных режимах позволяет сократить объем менструального кровотечения, особенно у пациенток с обильными менструальными кровотечениями и пройоменореей, и способствует профилактике эндометриоза. При альгодисменорее эксперты допускают назначение КОК в качестве препаратов первой линии терапии.
В такой ситуации крайне важно помнить, что в отсутствие положительного результата или при возникновении непреодолимых побочных эффектов эксперты рекомендуют дополнительное обследование и смену метода консервативной терапии. Длительность консервативной терапии эндометриоза, в частности, приема КОК, также регламентирована: до менопаузы. Однако и это положение в настоящее время подвергается сомнению, и существуют рекомендации о более длительной противорецидивной терапии, например, препаратом диеногест.
Особенность механизма действия комбинированных гормональных контрацептивов — антигонадотропный эффект, следствием которого являются подавление фолликулогенеза, блокада овуляции и вместе с этим уменьшение выброса в полость малого таза медиаторов воспаления, уменьшение синтеза активной фракции эстрогенов, а также антипролиферативное действие как на эутопический эндометрий, так и на эндометриоидные гетеротопии. Это позволяет предположить патогенетическую обоснованность включения комбинированных гормональных контрацептивов в арсенал средств для медикаментозной терапии эндометриоза. Уменьшение длительности и объема менструальной кровопотери на фоне приема комбинированных гормональных контрацептивов, достижение аменореи при применении пролонгированных режимов обеспечивают противорецидивное действие препаратов [7, 8].
В последние годы благодаря расширению возможностей малоинвазивной хирургии в ранней диагностике эндометриоза появились данные об отрицательном влиянии длительного применения комбинированных эстроген-гестагенных контрацептивов на течение заболевания [9]. Основную роль в неблагоприятном лечебном эффекте приписывают наличию эстрогенного компонента в комбинированном препарате, прогестерон-резистентности эндометриоидных гетеротопий и традиционному циклическому режиму применения гормональных контрацептивов [9].
В 2011 г. впервые опубликованы результаты систематического обзора и метаанализа различных исследований, проведенных за четыре десятилетия, согласно которым отмечено, что частота диагностики эндометриоза у пациенток, использовавших КОК на момент исследования, на 40% ниже (относительный риск (ОР) 0,63; 95% доверительный интервал (ДИ) 0,47—0,85), чем у женщин, недавно отменивших КОК (ОР 1,21; 95% ДИ 0,94—1,56), и у тех, кто когда-либо использовал КОК (ОР 1,19; 95% ДИ 0,89—1,6) [10]. Таким образом, высказано предположение о том, что купирование болевого синдрома на фоне приема комбинированного гормонального контрацептива, возможно, задерживает диагностику заболевания и уменьшает эффективность его хирургического лечения за счет «маскировки» симптомов эндометриоза. Данное предположение подтверждено в другом исследовании, в котором показано, что при эмпирическом назначении КОК с целью лечения первичной тяжелой дисменореи вероятность обнаружения эндометриоза у женщин, когда-либо применявших КОК, увеличивалась (скорректированное отношение шансов (ОШ) 2,79; 95% ДИ 1,74—5,12). При этом в наибольшей степени увеличивалась вероятность обнаружения глубоких инфильтративных форм заболевания (ОШ 16,2; 95% ДИ 7,8—35,3). Важно, что ни возраст начала применения, ни интервал времени после отмены гормональных контрацептивов у женщин контрольной группы и пациенток с подтвержденным диагнозом эндометриоз существенно не отличались. При этом минимальную вероятность интраоперационного обнаружения эндометриоидных гетеротопий имели женщины, применяющие гормональные контрацептивы в настоящее время (ОШ 1,22; 95% ДИ 0,6—2,52) [11]. Авторы данных метаанализов в заключение отмечают, что комбинированные гормональные контрацептивы не являются причиной развития эндометриоза. Скорее всего, сама первичная тяжелая дисменорея должна рассматриваться как маркер заболевания, а симптоматический лечебный эффект препарата, назначенного в стандартном циклическом режиме, в какой-то степени снижая выраженность болевого синдрома, становится причиной отсроченной диагностики и уменьшает шансы полноценного хирургического лечения эндометриоза. Об этом факте важно помнить практикующим врачам, так как согласно результатам опубликованных в 2017 г. пяти исследований с вовлечением 1187 женщин, задержка с установлением диагноза от начала появления первых симптомов заболевания составляет 8,6 года [12].
В последнее время в литературе появляется все больше данных о недостаточной эффективности КОК при лечении эндометриоза. В 2011 г. впервые опубликованы результаты интервью с использованием on-line-опроса 441 пациентки с НГЭ из 8 стран, включая США и Канаду. Возрастной диапазон опрошенных составил от 15 до 49 лет. Согласно полученным данным, около 70% пациенток указали на факт вынужденной смены нескольких КОК в связи с их недостаточной эффективностью в отношении купирования тазовой боли, связанной с эндометриозом. При этом более чем 40% пациенткам с НГЭ рекомендованы от 3 до 10 различных КОК с целью достижения лечебного эффекта [13].
Известно, что медикаментозная терапия эндометриоза должна быть непрерывной и длительной. В то же время клиницисту важно помнить, что в отсутствие достаточного клинического эффекта от проводимой эмпирической терапии комбинированными гормональными контрацептивами в течение 4—6 мес. целесообразно предложить пациентке переход на прием прогестагенов. В отсутствие эффекта даже у пациентки молодого возраста необходимо пересмотреть консервативную тактику ведения заболевания в пользу хирургического лечения. После проведения полноценного оперативного вмешательства чрезвычайно важно продолжить медикаментозную терапию эндометриоза с целью профилактики рецидивов заболевания. Если при этом пациентка не планирует беременность и нуждается в надежной контрацепции, препаратом выбора должен быть микродозированный (по дозе эстрогенного компонента) комбинированный гормональный контрацептив [14]. Это подтверждают результаты проведенного метаанализа 15 рандомизированных контролируемых исследований, включивших более 1800 пациенток после хирургического лечения эндометриом яичников. Отмечена значительно более низкая частота рецидивов на фоне гормональной терапии, чем без нее. При этом статистически значимой разницы между противорецидивной эффективностью КОК, гестагенов, агонистов гонадотропин-рилизинг-гормона (аГнРГ) не было. Однако при применении КОК частота побочных эффектов была значительно меньше, что обеспечило длительность терапии [15].
Несмотря на то что в течение более чем сорокалетнего периода сложилось мнение об эффективности устранения эндометриоз-ассоциированного болевого синдрома на фоне применения КОК, накопление данных и метаанализ проведенных исследований позволили заключить, что на сегодняшний день не существует убедительных доказательств эффективности КОК в отношении боли, ассоциированной с эндометриозом, по сравнению с плацебо или другими методами лечения. В литературных источниках последних лет приведены противоречащие друг другу данные об эффективности применения КОК у больных НГЭ. В 2018 г. представлены результаты, подтверждающие уменьшение эндометриоз-ассоциированного болевого синдрома, снижение риска рецидива и улучшение качества жизни на фоне применения КОК (систематический обзор 518 доступных источников, из которых 18 включены в обзор, из них 9 рандомизированы) [16].
Однако в 2019 г. опубликован обзор оценки эффективности применения КОК у женщин с эндометриозом, авторы которого отметили низкое качество большинства существующих исследований и их несоответствие требованиям рандомизации [17]. Только три из них были слепыми [18—20], в них подтверждалось снижение выраженности болевого синдрома на фоне применения КОК, однако не исключался эффект плацебо, особенно в исследованиях короткой продолжительности. Именно поэтому изучение эффективности применения КОК, модификации схем и путей введения препаратов должно быть продолжено, что доказывается большим количеством противоречивых данных в настоящее время. В последние годы появляется все больше сомнений в целесообразности применения КОК, особенно при глубоком инфильтративном эндометриозе и экстрагенитальных формах заболевания, в частности колоректального эндометриоза, когда более целесообразна, с точки зрения минимизации риска окклюзии кишечника, монотерапия прогестагенами. [21]. Существует мнение о том, что во всех случаях, когда КОК неэффективны при болевом синдроме, при появлении побочных эффектов или выявлении противопоказаний к применению гормональных контрацептивов, а также при глубоких инфильтративных формах, когда требуется более эффективное подавление активности эктопического эндометрия, целесообразно применение прогестагенов [22].
В ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» проведен ретроспективный анализ эффективности различных видов гормональной терапии у 1113 больных НГЭ после оперативного лечения, наблюдающихся в Центре диагностики и лечения эндометриоза. Выбор гормональной терапии был следующий: 573 пациентки получали терапию аГнРГ 6 циклов, 464 больных — диеногест 2 мг в течение 6 мес, 176 пациенток — КОК в стандартном режиме (преимущественно содержащие 30 мкг этинилэстрадиола) — 6—8 мес.
Частота рецидивов заболевания у пациенток, получавших комбинированные контрацептивы для терапии эндометриоза, оказалась наиболее высокой и составила 67,1%, после терапии аГнРГ — 14,3%, после применения диеногеста 2 мг — 11,9%. Из 229 больных с НГЭ III—IV степени после оперативного лечения наиболее высокий процент рецидивов обнаружен при применении КОК в циклическом режиме. На основании проведенной second-look лапароскопии установлено, что рецидивы НГЭ у пациенток, получавших диеногест-содержащий комбинированный контрацептив с этинилэстрадиолом 30 мкг в циклическом режиме после предыдущего оперативного лечения, в большинстве случаев сопровождались иссечением эндометриоидных инфильтратов, которые отсутствовали при проведении первой лапароскопии [23]. Аналогичные данные получены в другом исследовании, авторы которого подтверждают недостаточную эффективность КОК для профилактики рецидивов НГЭ и рекомендуют их назначать только с контрацептивной целью [24].
Безусловно, эффективность медикаментозной терапии и частота рецидивов зависят от качества выполненного оперативного лечения. Однако вопросы схем применения и состава препаратов для консервативной терапии подлежат дальнейшему изучению с целью расширения доказательности. В настоящее время уже накоплены и опубликованы данные метаанализов эффективности применения КОК в пролонгированных режимах [25]. По сравнению с циклической схемой применения КОК, непрерывный режим демонстрирует большую эффективность при использовании для предупреждения рецидивов эндометриоидных кист яичников, лечения дисменореи и купирования хронической тазовой боли, но не имеет статистически значимых отличий при лечении такого симптома как диспареуния [26]. К непрерывному режиму (или пролонгированной схеме) применения КОК относятся такие длительное время применяемые в практике схемы, как 48/4, 72/4, 63/7, 84/7, в которых первая цифра обозначает количество активных таблеток, а вторая цифра — количество дней перерыва в приеме активных таблеток.
Однако, исходя из нашего опыта, пациенткам с эндометриозом мы не рекомендуем даже при пролонгированном режиме приема КОК делать 7-дневный перерыв в приеме препарата. Известно, что при применении комбинированных контрацептивов с 7-дневным перерывом уже с 4-го дня этого перерыва происходит рост фолликула, который при достижении размеров 8—10 мм обладает собственной зависимой от фолликулостимулирующего гормона ароматазной и, следовательно, эстрогенной активностью. Именно по этой причине мы рекомендуем применять «пролонгированный» режим (например, схемы 72/4 или 63/4). Целесообразно пациенткам с эндометриозом назначать монофазные препараты с минимальной дозой эстрогенного компонента. Возможен выбор препаратов, содержащих прогестаген, с мощным антипролиферативным потенциалом. В настоящее время официально зарегистрирован микродозированный препарат, содержащий этинилэстрадиол 20 мкг в сочетании с активным производным 19-нортестостерона — левоноргестрелом (ЛНГ). Препарат рекомендуется к применению в пролонгированном режиме: 84 дня с последующим назначением комбинированных контрацептивов с коротким 4-дневным перерывом, приемом в течение 7 дней этинилэстрадиола 10 мкг с целью пролонгирования антигонадотропной и, как следствие, антиэстрогенной эффективности препарата.
Препаратом выбора также могут стать контрацептивы, содержащие эстрогены, биоидентичные натуральным, в сочетании с прогестагенами, например, диеногестом или номегестрола ацетатом. Однако отдаленных результатов об эффективности длительных, «пролонгированных» схем комбинированных контрацептивов с коротким межкурсовым перерывом у больных НГЭ в настоящее время нет, поэтому требуется дальнейшее изучение этого вопроса.
В настоящее время не опубликовано ни одного рандомизированного исследования об использовании комбинированных контрацептивов (КК) в виде кольца или пластыря для лечения эндометриоз-ассоциированной боли. Однако, по данным проспективного когортного исследования, такие КК как вагинальное кольцо (этинилэстрадиол 15 мкг и этоногестрел 120 мкг), так и трансдермальный пластырь (этинилэстрадиол 20 мкг и норэлгестрамин 150 мкг) продемонстрировали уменьшение выраженности рецидивирующего болевого синдрома после хирургического лечения эндометриоза, при этом использование кольца было более эффективным [27]. В литературе также описывается использование вагинального кольца (этинилэстрадиол 15 мкг и этоногестрел 120 мкг) с целью снижения болевого синдрома, ассоциированного с глубоким инфильтративным эндометриозом. Результаты продемонстрировали сравнимую с применением дезогестрела (75 мкг ежедневно) эффективность [28].
Обсуждающийся риск пролиферативного действия на эндометриоидные очаги эстрогенного компонента комбинированных гормональных контрацептивов, а также возможный риск тромботических осложнений у пациенток, имеющих противопоказания к применению эстрогенов, стали причиной изучения лечебного действия прогестин-содержащих гормональных контрацептивов при эндометриозе. Сравнительная оценка уровня эстрадиола в крови показала, что во время естественного овуляторного менструального цикла уровень циркулирующего эстрадиола колеблется в широких пределах: от 30 пг/мл (110,1 пмоль/л) до 140 пг/мл (513,9 пмоль/л); в то время как при ежедневном применении диеногеста в дозе 2 мг содержание эстрадиола остается стабильным в пределах 30—60 пг/мл (110,1—220,2 пмоль/л) [29]. Существуют данные о том, что при использовании комбинации диеногеста и эстрадиола валерата в четырехфазном режиме в течение менструального цикла достигается более высокая, но стабильная концентрация эстрадиола — 80 пг/мл (293,7 пмоль/л). При применении диеногеста с этинилэстрадиолом в монофазном режиме средний уровень эстрадиола на протяжении всего цикла опускается еще ниже (30—70 пг/мл или 110,1—257,0 пмоль/л). Но при этом регистрируются ежедневные пики 100—130 пг/мл (367,1—477,3 пмоль/л) сразу после окончания приема препарата, что, вероятно, может способствовать стимуляции эндометриоидных гетеротопий [30, 31].
Считается, что прогестины следует назначать больным, у которых не получен положительный эффект от лечения или обнаружены непреодолимые побочные эффекты на фоне применения эстроген-гестагенных препаратов, а также больным с диспареунией и/или глубокими инфильтративными формами эндометриоза [9].
С учетом доказанной безопасности, достаточного клинического эффекта при лечении эндометриоз-ассоциированной тазовой боли, предупреждения прогрессирования заболевания, а также с целью контрацепции назначение только прогестаген-содержащих препаратов (например, дезогестрел- или этоногестрел-содержащих) [32, 33] данным больным более предпочтительно, чем назначение комбинированных гормональных контрацептивов [34].
Однако следует предупреждать пациенток о таких побочных эффектах на фоне их применения, как межменструальные кровянистые выделения, вплоть до кровотечений прорыва, что может снизить приверженность к данному виду терапии.
Применение внутриматочной системы с ЛНГ (ЛНГ-ВМС) у больных инфильтративным эндометриозом, как показано в ряде исследований, приводит к значительному снижению интенсивности тазовых болей, дисменореи, диспареунии и уменьшению размеров эндометриоидного инфильтрата [35]. ЛНГ-ВМС представляет собой Т-образную внутриматочную спираль, содержащую контейнер с 52 мг ЛНГ, локальное внутриматочное выделение которого в дозе 30 мкг/24 ч обеспечивает антипролиферативный эффект на эндометрий. Поскольку уровень прогестагена в крови при внутриматочном использовании ЛНГ ниже, чем при применении оральных прогестагенов, системные побочные эффекты являются менее выраженными, что является дополнительным преимуществом использования этого метода.
Результаты повторной лапароскопии показали уменьшение числа эндометриоидных гетеротопий у 60% пациенток, использовавших ЛНГ-ВМС [36]. Однако патогенетические механизмы влияния внутриматочной системы на генитальный эндометриоз остаются неизвестными. При проведении отсроченной повторной лапароскопии отмечено, что у больных эндометриозом на фоне внутриматочной системы уменьшается объем перитонеальной жидкости, а содержание ЛНГ в ней составляет 2 /3 от его уровня в сыворотке крови, что может объяснить механизм снижения интенсивности тазовых болей [37].
На фоне применения ЛНГ-ВМС отмечается снижение экспрессии в железах и строме эндометрия фактора роста эндотелия сосудов (VEGF), что обусловливает его антиангиогенное влияние и патогенетическую обоснованность применения при эндометриозе [38]. Локальный эффект ЛНГ на эндометрий проявляется гипоменореей или аменореей, значительно уменьшающей болевой синдром и выраженность меноррагии. Однако ЛНГ-ВМС система не обладает антигонадотропным действием, поэтому для пациенток с функциональными кистами яичников в анамнезе данный вид терапии не должен рассматриваться как приоритетный.
Представленные результаты доказывают положительное влияние длительного использования данного вида терапии у женщин с симптомами эндометриоза (в том числе при сочетании аденомиоза с НГЭ).
Одним из перспективных направлений в контрацепции у больных эндометриозом является создание рилизинговой системы в виде кольца для интравагинального применения, в состав которого входят ингибитор ароматазы анастразол и прогестаген ЛНГ. Данный препарат позиционируется как для контрацепции, так и для длительного лечения эндометриоза [39].
Заключение
Обзор имеющихся в настоящее время исследований позволяет считать целесообразным назначение пациенткам с подозрением на эндометриоз, нуждающимся в контрацепции, микродозированных по дозе эстрогенного компонента комбинированных гормональных контрацептивов. Препаратом выбора также могут стать контрацептивы, содержащие в своем составе эстрогены, биоидентичные натуральным. При этом важным является выбор пролонгированного режима приема. Однако при сохранении болевого синдрома на фоне применения комбинированных контрацептивов необходимо предложить переход на прогестагены. В отсутствие эффекта даже у пациенток молодого возраста следует пересмотреть консервативную тактику ведения в пользу хирургического лечения. Больным с глубоким инфильтративным эндометриозом или экстрагенитальным эндометриозом эстроген-прогестагенные контрацептивы применять не рекомендуется; можно назначать только прогестаген-содержащие препараты.
В каждом конкретном случае состав препаратов и схемы их применения должны быть индивидуально подобраны, а эффективность модифицированных схем консервативной терапии больных с эндометриозом подлежит дальнейшему изучению с целью расширения доказательности.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.