Как называется вода в газообразном состоянии
Водяной пар — газообразное состояние воды
Водяной пар играет важнейшую роль в жизни нашей планеты в целом и в жизни человека в частности …
Водяной пар — газообразное состояние воды
Водяной пар — это вода в газообразном состоянии. Газообразное состояние относится к трем основным агрегатным состояниям воды, встречающихся в природе в естественных условиях. Чистый водяной пар не имеет ни цвета, ни вкуса. Наибольшее скопление пара наблюдается в тропосфере.
Приведём еще одно определение из справочника.
Водяной пар — вода, содержащаяся в атмосфере в газообразном состоянии. Количество водяного пара в воздухе сильно меняется; наибольшее его содержание – до 4 %. Водяной пар невидим; то, что называют паром в быту (пар от дыхания на холодном воздухе, пар от кипения воды и т. п.), – это результат конденсации водяного пара, как и туман. Количество водяного пара определяет важнейшую для состояния атмосферы характеристику – влажность воздуха.
География. Современная иллюстрированная энциклопедия. — М.: Росмэн. Под редакцией проф. А. П. Горкина. 2006
Как образуется водяной пар
Образование пара происходит в результате двух процессов – испарения или кипения. При испарении пар образуется только на поверхности вещества, при кипении же пар образуется по всему объему жидкости, о чем и свидетельствуют пузырьки, активно поднимающиеся вверх во время процесса кипения.
Кипение воды происходит при температурах, которые зависят от химического состава водного раствора и атмосферного давления. Температура кипения остается неизменной на протяжении всего процесса.
Насыщенный пар
Пар, образующийся в результате кипения, называется насыщенным. Насыщенный пар в свою очередь подразделяется на насыщенный сухой и насыщенный влажный пар. Насыщенный влажный пар состоит из взвешенных капелек воды, температура которых находится на уровне кипения, и соответственно самого пара, а насыщенный сухой пар не содержит капелек воды.
Перегретый пар
Так же существует «перегретый пар», который образуется при дальнейшем нагреве влажного пара, этот вид пара обладает более высокой температурой и более низкой плотностью.
Использование пара человеком
С паром мы постоянно сталкиваем в ежедневной жизни, он появляется — над носиком чайника при кипении воды, при глажке, при посещении бани… Однако не забывайте, что, как мы уже отмечали выше, чистый водяной пар не имеет ни цвета, ни вкуса.
Благодаря своим физическим свойствам и качествам, пар уже давным-давно нашел свое практическое применение в хозяйственной деятельности человека. И не только в быту, но и при решении больших глобальных задач. Долгое время пар был главной движущей силой прогресса как в прямом, так и в переносном смысле этого выражения. Он использовался как рабочее тело паровых машин, самой известной из которых является ПАРОВОЗ.
Пар и в наше время широко используется в хозяйственных и производственных нуждах:
Значение водяного пара для экосистемы Земли и его влияние на климат нашей планеты
Водяной пар активно участвует в создания парникового эффекта на Земле. Его влияние на климат планеты весьма значительно. Поэтому к нему приковано внимание многих ученых, занимающихся данной проблематикой.
Водяной пар активно участвует во многих химических процессах происходящих в атмосфере, стратосфере, топосфере.
Водяной пар является незаменимым элементом такого важного для нашей планеты процесса как Круговорот воды в природе (глобальный гидрологический цикл). Повышение интенсивности круговорота воды в природе приведет к весьма плачевным для человечества результатам — экстремальные осадки, наводнения, засухи …
Выводы
Подводя итоги, отметим, что, несмотря на всю свою «незаметность», водяной пар является не только важным элементом глобальной эко-системы Земли, но так же и весьма полезным веществом для хозяйственной и экономической деятельности человека.
Агрегатное состояние воды

Всего получено оценок: 134.
Всего получено оценок: 134.
Вода — важная составляющая нашей планеты, основа жизни на Земле. В природе она может находиться в трёх разных агрегатных состояниях: твёрдом, жидком и газообразном. Примеры этих состояний можно наблюдать в погодных явлениях. В статье кратко опишем, как происходит процесс перехода воды из одного состояния в другое, что на это влияет.
Твёрдое состояние воды
В твёрдом состоянии вода представляет собой лёд, снег и иней. При низкой температуре жидкая вода замерзает, и её молекулы начинают приобретать форму кристаллов. Чтобы вода начала замерзать, достаточно 0 °С по Цельсию, и ниже.
При замерзании молекулы воды отодвигаются друг от друга, делая лёд менее плотным, чем жидкость. Это значит, что вода в твёрдом состоянии имеет больший объём, чем в жидком.
Большинство веществ при снижении температуры сжимается, а вода — расширяется, и в этом заключается её уникальная особенность. В качестве доказательства можно наполненную водой бутылку поставить в морозильник. Когда вода превратиться в лёд, её объём увеличится, и бутылка попросту взорвётся.
Наличие солей в воде снижает температуру замерзания. По этой причине солёная морская вода замерзает не при О °С, а при –1,8 °С по Цельсию.
Жидкое состояние воды
Вода в жидком состоянии широко распространена по всей планете. Это не только реки, моря и озера, но также атмосферные осадки (дождь) и облака, которые состоят из крошечных капелек воды. Кроме того, вода в жидком агрегатном состоянии вода находится в почве в виде подземных рек и озёр.

Жидкая вода с лёгкостью переходит в газообразное и твёрдое состояние под воздействием температуры. В этом процессе свою роль играет и давление.
Газообразное состояние воды
Переход воды из жидкого состояния в газообразное называется испарением. В условиях нормального атмосферного давления он происходит при 100 °С по Цельсию (для пресной воды).
При кипячении вода из состояния жидкости переходит в пар — газообразное состояние воды. В природе вода также испаряется с поверхности водоёмов, просто этот процесс происходит гораздо медленнее. Скорость испарения зависит от температуры. Вода, испарённая с поверхности Земли, образует облака и тучи.

Помимо основных трех форм, вода может находиться в четвёртом агрегатном состоянии — плазмы, или, точнее, гидроплазмы. Если водяной пар нагреть до температуры 2200–13900 °С по Цельсию, то молекулы воды начнут распадаться, и в результате получится смесь атомов кислорода и водорода в виде плазмы.
Что мы узнали?
Существуют три состояния воды в природе: жидкое, твёрдое и газообразное. На переход из одного состояния в другое влияют внешние факторы, прежде всего, температура. Также существует четвёртое состояние воды — плазма, однако для неё нужно соблюдать экстремально высокую температуру, которую можно обеспечить лишь в лабораторных условиях. Для учеников 3 класса на уроке по окружающему миру можно кратко перечислить понятные примеры агрегатных состояний: дождь, облака (жидкое), лёд, иней, снег (твёрдое), пар (газообразное).
Агрегатные состояния воды в обычных условиях
Агрегатные состояния воды в природе — облака, дождь, снег, лед, град, роса, иней туман … мы знакомы с ними с раннего детства.
Агрегатные состояния воды в обычных условиях в природе
Агрегатные состояния воды ежедневно встречаются нам в окружающей нас природе. Они активно влияют на все аспекты жизнедеятельности человека.
В природе в естественных условиях вода может в изобилии существовать в 3-х основных агрегатных состояниях:
Круговорот воды в природе
Жидкое состояние воды в природе
Без воды в жидком состоянии большинство живых существ на нашей планете просто погибнет.
Аккумулируется вода в жидком состоянии в хорошо всем нам известных формах — это океаны, моря, реки, озёра, пруды, ставки, каналы, атмосферных осадках …
Отметим интересный факт — вода в жидком состоянии при фиксированном объёме не имеет фиксированной формы.
Твердое состояние воды в природе
Вода из жидкого состояния переходит в твердое при температуре 0º C (плюс/минус в зависимости от давления). Процесс перехода воды из жидкого состояния в твердое имеет интересную аномалию. При понижении температуры молекулы воды, как и в других материях, сближаются друг с другом. Так происходит вплоть до температуры 4º C. При этой температуре у воды максимальная плотность. При дальнейшем понижении температуры плотность начинает уменьшаться. Благодаря именно этому удивительному свойству лёд плавает, а не тонет. Плотность льда составляет приблизительно 90% от плотности воды.
Вода в твердом состоянии имеет как фиксированный объём, так и фиксированную форму.
Газообразное состояние воды в природе
Из жидкого состояния в парообразное вода переходит при температуре 100º C (плюс/минус в зависимости от давления). Водяной пар не всегда можно увидеть, но его можно почувствовать. Количество пара в атмосфере определяется как влажность. При повышенной влажности можно сказать, что по ощущениям воздух становится «липким».
Агрегатные состояния воды — переходные процессы
Процессы перехода воды с одного агрегатного состояния в другое определяются следующим образом:
Граничные точки перехода воды в состояния лед/вода и вода/пар определили соответственно как 0 и 100 градусов по Цельсию при условии атмосферного давления 760 мм рт. ст. или 101 325 Па. Всем с детства хорошо известна простая примета, температура за окном опустилась ниже нуля, ждите снега 🙂
Четвёртое или второе жидкое агрегатное состояние воды
Относительно недавно физики обнаружили новое состояние воды. Это состояние проявляется при температурах в промежутке от 40º до 60º C и проявляется в том, что жидкая вода непрерывно переключается между двумя состояниями, которые имеют разный набор физических свойств.
Важно знать …
Необходимо отметить такой, важный для человека факт – при понижении атмосферного давления температура кипения падает. Это необходимо учитывать, например, в условиях высокогорья. Отметим также еще одно явление, которое полезно знать человеку в повседневной жизни — объем воды в твердом состоянии больше чем в жидком. Этот факт иллюстрирует общеизвестный пример – бутылка с водой оставленная на морозе будет разорвана, образовавшимся в ней льдом.
Очевидно, что в разных своих агрегатных состояниях Вода обладает разными базовыми физическими свойствами такими как – текучесть, твердость, летучесть.
Необходимо отметить, что пар определяет такой важный для человека и других живых организмов параметр как «влажность воздуха«. Влажность воздуха напрямую зависит от количества водяного пара в атмосфере, больше пара выше влажность. На земле существуют места как с очень высокой, так и с низкой влажностью атмосферы. Одним из самых влажных мест планеты считается индийский город Черрапунджи (Cherrapunji), а одним из самых сухих Сухие долины в Антарктике.
Выводы
Еще раз сделаем акцент на том, что во многом благодаря именно способности воды находиться в природных естественных условиях в трех разных агрегатных состояниях и существует жизнь на нашей планете.
Испарение, конденсация, кипение. Насыщенные и ненасыщенные пары
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. Переход из одного состояния в другое называется фазовым переходом. Испарение и конденсация являются примерами фазовых переходов.
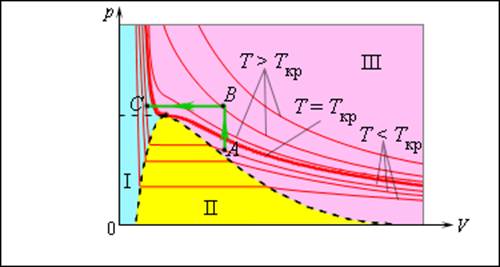
Все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость. Однако такое превращение может происходить только при температурах ниже определенной, так называемой критической температуры Tкр. Например, для воды критическая температура равна 647,3 К, для азота 126 К, для кислорода 154,3 К. При комнатной температуре (≈ 300 К) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов.
Испарением называется фазовый переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости (если нет подвода энергии от окружающих тел).
Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
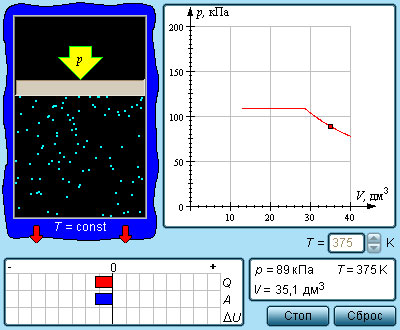 | |||
| Испарение | Кипение |
| При любой температуре, с поверхности жидкости | При определенной температуре, во всем объеме жидкости |
Испарение на уровне молекул
Давайте вспомним об особенностях разных агрегатных состояний вещества.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
Из этой таблицы видно, что молекулы в жидкостях находятся близко друг другу, но хаотично, то есть не имеют кристаллической решетки, как в твердых телах. Эти молекулы движутся (причем, чем выше температура, тем быстрее движутся) и в ходе движения сталкиваются. Столкновения меняют направление и скорость движения — из-за этого молекулы иногда быстро устремляются к поверхности жидкости и вылетают из нее. Это и есть испарение.
В предыдущем абзаце мы не случайно заметили, что молекулы движутся быстрее при увеличении температуры — ведь из-за этого испарение идет интенсивнее. В этом случае происходит охлаждение: нагретую жидкость уже покинули все самые быстрые молекулы и температура самой жидкости понижается.
Интенсивность испарения
Интенсивностью испарения называют количество воды, которое испаряется с поверхности площадью 1 см2 за одну секунду.
Интенсивность испарения зависит от следующих факторов:
Скорость испарения — количество жидкости, которая испаряется со свободной поверхности в единицу времени.
Интенсивность испарения — количество жидкости, которая испаряется с единицы площади поверхности в единицу времени.
По сути, это два очень близких друг к другу понятия, поэтому разница будет лишь в величинах и единицах измерения, а суть процесса отражают обе формулировки.
Насыщенный пар
Процесс испарения напрямую связан с круговоротом воды в природе. Вода, испаряясь, превращается в водяной пар и поднимается вверх, где происходит конденсация пара, образуются облака, и вода возвращается на землю в виде осадков.
Вследствие конденсации водяного пара, который живет в воздухе, образуются облака и туман. По этой же причине холодное стекло запотевает, соприкасаясь с теплым воздухом.
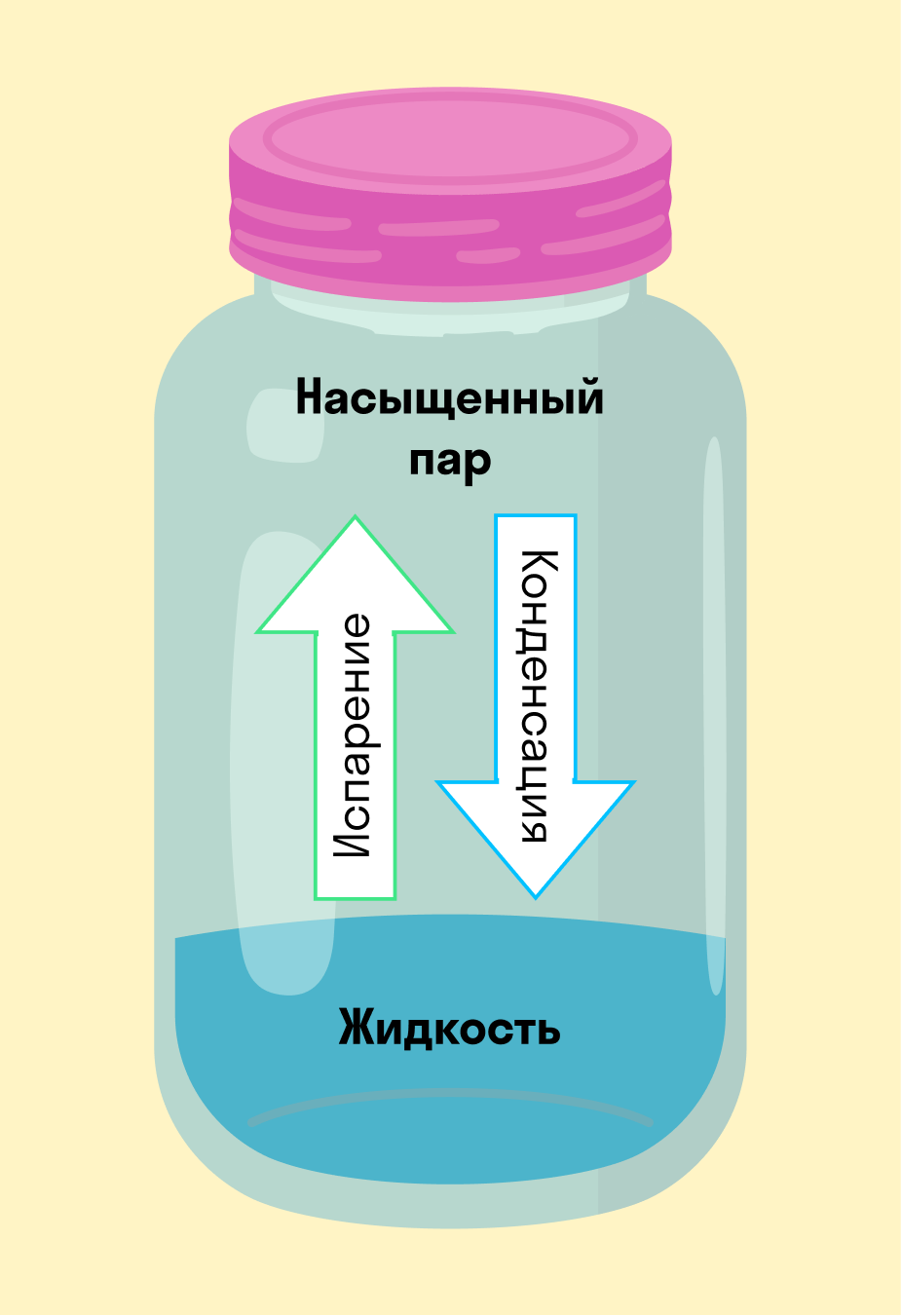
На рисунке — процессы испарения и конденсации в плотно закрытом сосуде, когда жидкость и пар находятся в динамическом равновесии. Это значит, что одновременно конденсируется и испаряется одинаковое количество вещества.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Но бесконечное количество пара в воздух не запихнешь. Поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Но если мы тот же воздух поместим в помещение с температурой +20 градусов, то в него может испариться уже до 17 миллиграмм пара. Значит его влажность будет равна 1/17 = 6%. Человеку комфортнее всего находиться при значении влажности 40-50%.
Попробуйте курсы подготовки к ЕГЭ по физике с опытным преподавателем в онлайн-школе Skysmart!
Испарение в жизни
И действительно: чего в этой жизни только не испаряется — мы встречаемся с этим каждый день. Давайте узнаем, зачем этот процесс вообще нужен, и как люди научились извлекать из него пользу.
Испарение в организме человека и животных
Выше мы разбирали вопрос, почему если облиться теплой водой, нам все равно станет холодно. По этому же принципу работает ощущение холода после того, как мы вспотели — в какой-то момент нам становится холодно.
Само потоотделение — важный процесс терморегуляции организма. Если мы достигаем высокой температуры (из-за внешних воздействий или же из-за болезни), то организм стремится себя охладить, чтобы не умереть из-за превращения белков в нашем организме в яичницу.
Пот выделяется через поры кожи, а затем испаряется — все это позволяет нашему организму быстро избавиться от лишней энергии, охладить тело и нормализовать температуру.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой и «скинуть» избыточное тепло, но при высокой влажности пот не может испариться.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно. А при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.
У животных этот механизм работает схожим образом. Но, например, собакам испарения с кожи недостаточно, поэтому они часто открывают пасть, высовывают язык и дышат порой ну очень смешно 🐶
Именно гортань и язык собаки идеально подходят для испарения влаги и охлаждения тела животного.
Испарение у растений
Удивительно, но у растений механизм испарения тоже работает схожим образом. Растения очень любят воду, поэтому домашние растения мы поливаем, а в пустынях их просто нет.
Ту воду, которую цветы поглотили, они могут испарять, чтобы не перегреться под жарким солнцем. Да, вода нужна, чтобы растения питались, но в жаркие дни еще и для температурной саморегуляции. Поэтому не забывайте поливать цветы, а в очень жаркие дни делайте это еще интенсивнее.
Испарение в природе и окружающей среде
Процесс испарения напрямую связан с круговоротом воды в природе. Именно круговоротом воды в природе обеспечивается жизнь на Земле — так как влага разносится по всему миру, растения в дикой природе способны жить без наших попыток полить большую пальму из леечки.
Испарение воды с поверхности рек, озер, морей и океанов создает дождевые тучи, которые затем, проливаясь дождем, поливают растения и деревья. Многие дождь не любят, мол, он мокрый, мерзкий и затекает в ботинки, но он очень нужен засушливым регионам — Северной Африке или Центральной Индии, которые часто страдают от засухи.
Испарение в промышленности и быту
С бытом совсем все просто: мы сушим вещи, готовим еду, покупаем увлажнители воздуха или размазываем разлитую лужу по полу.
В случае с промышленностью для нас все не так очевидно. Промышленная техника, работающая на основе испарения, разрабатывается по схожей схеме: в ней всегда максимально увеличена площадь поверхности жидкости, чтобы испарение шло интенсивно.
Например, испаритель, изображенный на схеме, состоит из совокупности соединенных между собой испарителей. В основе его действия — пар, полученный в одной ступени, который используют в качестве источника тепла для следующей ступени. По мере того, как температура уменьшается от одной ступени к другой, вакуум увеличивается, так что температура кипения становится ниже и испарение поддерживается. Он предназначен для того, чтобы очистить воду от отходов.
- Как оборудовать место для ночлега собаки своими руками: практическое руководство
- посадить пихту на участке примета