как сильно можно сжать воду
Как сильно можно сжать воду
Войти
Авторизуясь в LiveJournal с помощью стороннего сервиса вы принимаете условия Пользовательского соглашения LiveJournal
Можно ли сжать воду?
Откуда же у воды эта колоссальная сила?
Надавим пальцем на небольшой булыжник. На нём не образуется ни малейшей вмятины. А в воду палец погрузится без всякого нажима. Кто знаком с физикой, сможет объяснить: нашей силы оказалось недостаточно, чтобы сжать камень. Вода же и не сжималась. Она лишь раздвинулась, вытеснилась пальцем и заняла новое место; при этом её уровень в сосуде повысился.
Значит ли это, что вода «слабее» камня?
В физической лаборатории можно произвести такой опыт: камень и примерно такой же объём воды попробовать сжать в мощном прессе. Надо воду налить в очень прочный стальной стакан и давить на её поверхность поршнем.
При определённой силе давления камень начнёт сжиматься, а затем крошиться, разрушаться. С водой же ничего не случится, если даже на неё давить с силой во много раз большей. При огромном давлении — около 10 000 тысяч атмосфер — вода сожмётся лишь на одну шестую часть своего объёма.
Этим свойством воды широко пользуются в технике, например в устройствах гидравлических прессов и подъёмников.
Плотной струёй воды, выбрасываемой из особых водяных пушек — гидромониторов, дробят пласты угля и торфа, гасят пламя пожаров. Специальные суда — земснаряды, используя силу воды, размывают природные грунты (песок, глину, гравий и др.), перекачивают их по трубам и в короткий срок намывают гигантские плотины, дамбы и т.п.
Огромная сила воды проявляется и при её охлаждении. Как действует холод на большинство веществ? Они сжимаются, становятся меньше по объёму. Это явление всегда учитывается при строительстве зданий, линий электропередач и т.п.
У воды — иное свойство. Когда она превращается в лёд, то расширяется, занимает больший объём. Вода, замёрзшая в горных расщелинах, легко раскалывает прочнейшие каменные массивы. Много раз бывало, что корпуса больших кораблей, вмёрзшие в полярные льды, раздавливались, как хрупкие скорлупки.
Источник: «Природа — мудрый конструктор» К. Курденков, Ю. Юркан. 1967 г.
1000 «детских» вопросов и ответов. (длиннопост) Ч. 8
95. Почему снег поглощает звуки?
Во время снегопада крики слышны на меньшее расстояние, чем в ясную погоду, свежий снежный покров тоже поглощает звук. Дело в том, что мелкие поры снежных хлопьев и рыхлого, недавно выпавшего снега приглушают звуковые волны. Они попадают в маленькие поры кристаллов снега и теряются там: их энергия пропадает. Старый снег или лед имеют гладкую поверхность и больше не могут так хорошо поглощать звук, а особенно далеко голоса разносятся над спокойной поверхностью воды.
97. В чем разница между водой и водяным паром?
Все вещества, с которыми мы встречаемся в окружающем нас мире, бывают или жидкими, или твердыми, или газообразными.
Эти состояния веществ называют агрегатными состояниями.
Многие вещества при охлаждении или нагревании можно перевести из одного агрегатного состояния в другое.
При этом они неожиданно приобретают совсем другие свойства.
Например, если нагреть воду до температуры выше 100 градусов Цельсия, она превращается в газ, в водяной пар.
У воды и водяного пара одинаковый химический состав, но совершенно разные свойства: водяной пар имеет свойства, типичные для газов.
Его можно сжимать, как воздух. Пар, как и воздух, обладает упругостью, он может сжиматься и снова расширяться и при этом может привести в действие паровую машину.
98. А есть жидкий воздух?
Даже такие прочные и твердые вещества, как железо, можно нагреть до такой температуры, что они становятся жидкими. При еще более высоких температурах жидкие металлы превращаются в газ. И наоборот, вещества, встречающиеся при нормальных температурах в виде газа, можно охладить до такой степени, что они становятся жидкими или даже твердыми. Например, воздух при температуре в минус 197,5 градуса Цельсия превращается в жидкость.
99. Почему дым поднимается вверх?
Дым содержит много мельчайших частиц, в том числе сажу, летучую золу и капельки смолы. Они возникают при сгорании. В ясную, сухую и безветренную погоду дым из трубы или от костра поднимается вертикально вверх. Тогда все содержащиеся в дыме вещества легкие и сухие и поднимаются вместе с горячим воздухом. Иначе обстоит дело в дождливую погоду. Тогда воздух влажный и содержит много водяного пара. Невидимые маленькие капельки, из которых состоит пар, оседают на частицах дыма и тянут дым вниз. Поэтому он становится тяжелым и не может так легко подниматься вверх. Если дым не поднимается над трубой, а висит над крышами, это — признак высокой влажности воздуха. Очень может быть, что скоро пойдет дождь.
100. Можно ли сжать воду?
Жидкости нельзя сжать. Они не обладают упругостью и не изменяют свой объем. Объемом предмета называется пространство, которое он занимает. Поэтому совершенно невозможно вместить два литра воды в литровую бутылку.
101. Почему губка впитывает воду?
На губке хорошо видно, как вода сама собой поднимается по маленьким щелочкам, тонким трубочкам и маленьким порам. В губке много маленьких пор. Если положить ее в пролитую воду, губка становится мокрой. Вода проникает в поры, и лужица пропадает. Это свойство воды называется капиллярностью (слово происходит от латинского «capillaris» — «волосной», потому что поры имеют толщину волоса). И промокательная бумага может впитывать воду только потому, что в ней много очень маленьких пор. Кстати, все полотенца и тряпки для вытирания имеют такое же строение. Гладкая бумага или гладкий шелк впитывают воду очень плохо.
102. Сколько воды нужно дереву?
Ни одно живое существо не может обойтись без воды. Животные пьют воду, берут ее из пищи или поглощают кожей. Растения впитывают воду главным образом корнями из почвы. Таким образом, большое дерево поглощает за сутки тонну воды, которая поднимается из корней по стволу и ветвям в листья и там испаряется.
103. Как вода попадает в крону дерева?
Это происходит без помощи мускулов или насоса. Дело в том, что вода сама поднимается по тонким трубочкам наверх. По древесине корней, ствола и ветвей проходит огромное количество таких трубочек и каналов. Они, как губка, впитывают воду.
Как только она испаряется с листьев, вверх всасывается новая вода.
Чем больше дерево, тем труднее ему поднимать наверх большое количество воды. Поэтому огромные секвойядендроны (Мамонтовы деревья) в Северной Америке произрастают только во влажных областях, где часто бывают обильные туманы. Они могут поглощать воду листьями из тумана.
104. Почему иголка может плавать?
Если осторожно положить иголку на воду, она не тонет, а плавает. Внимательно присмотревшись, можно увидеть, что иголка сделала в поверхности воды небольшое углубление, это выглядит так, словно на поверхности воды натянута тонкая пленка, а на ней лежит иголка. То, что выглядит как пленка и удерживает иголку на поверхности, — это поверхностное натяжение воды.
Молекулы воды стараются находиться как можно ближе и притягиваются друг к другу, «натягивая» поверхность воды. Правда, сила поверхностного натяжения очень мала, но она может вытолкнуть такой легкий предмет, как иголка. Но как только один конец иглы опустится в воду, чары разрушатся, поверхностное натяжение исчезнет, и иголка утонет.
А для предметов более тяжелых, чем иголка, сила поверхностного натяжения воды слишком мала.
105. Почему на старых фотографиях люди так напряженно смотрят в объектив?
У первых фотографов людям приходилось целую минуту сидеть неподвижно перед фотоаппаратом, пока фотопленки того времени освещались. Если человек шевелился или хотя бы мигал, изображение получалось нечетким — отсюда и напряженные позы.
Особенно неприятно это было для детей. Они не могут так долго сидеть неподвижно, и фотографам часто приходилось повторять съемку. Поэтому за фотопортреты детей просили больше денег, чем за фотографии взрослых.
Предложена новая теория, объясняющая, почему вода при нагревании от 0 до 4°C сжимается
Японский физик Масакадзу Мацумото выдвинул теорию, которая объясняет, почему вода при нагревании от 0 до 4°C сжимается, вместо того чтобы расширяться. Согласно его модели, вода содержит микрообразования — «витриты», представляющие собой выпуклые пустотелые многогранники, в вершинах которых находятся молекулы воды, а ребрами служат водородные связи. При повышении температуры конкурируют между собой два явления: удлинение водородных связей между молекулами воды и деформация витритов, приводящая к уменьшению их полостей. В диапазоне температур от 0 до 3,98°C последнее явление доминирует над эффектом удлинения водородных связей, что в итоге и дает наблюдаемое сжатие воды. Экспериментального подтверждения модели Мацумото пока что нет — впрочем, как и других теорий, объясняющих сжатие воды.
В отличие от подавляющего большинства веществ, вода при нагревании способна уменьшать свой объем (рис. 1), то есть обладает отрицательным коэффициентом теплового расширения. Впрочем, речь идет не обо всём температурном интервале, где вода существует в жидком состоянии, а лишь об узком участке — от 0°C примерно до 4°C. При больших температурах вода, как и другие вещества, расширяется.
Между прочим, вода — не единственное вещество, имеющее свойство сжиматься при увеличении температуры (или расширяться при охлаждении). Подобным поведением могут «похвастать» еще висмут, галлий, кремний и сурьма. Тем не менее, в силу своей более сложной внутренней структуры, а также распространенности и важности в разнообразных процессах, именно вода приковывает внимание ученых (см. Продолжается изучение структуры воды, «Элементы», 09.10.2006).
Некоторое время назад общепринятой теорией, отвечающей на вопрос, почему вода увеличивает свой объем при понижении температуры (рис. 1), была модель смеси двух компонент — «нормальной» и «льдоподобной». Впервые эта теория была предложена в XIX веке Гарольдом Витингом и позднее была развита и усовершенствована многими учеными. Сравнительно недавно в рамках обнаруженного полиморфизма воды теория Витинга была переосмыслена. Отныне считается, что в переохлажденной воде существует два типа льдообразных нанодоменов: области, похожие на аморфный лед высокой и низкой плотности. Нагревание переохлажденной воды приводит к плавлению этих наноструктур и к появлению двух видов воды: с большей и меньшей плотностью. Хитрая температурная конкуренция между двумя «сортами» образовавшейся воды и порождает немонотонную зависимость плотности от температуры. Однако пока эта теория не подтверждена экспериментально.
С приведенным объяснением нужно быть осторожным. Не случайно здесь говорится лишь о структурах, которые напоминают аморфный лед. Дело в том, что наноскопические области аморфного льда и его макроскопические аналоги обладают разными физическими параметрами.
Японский физик Масакадзу Мацумото решил найти объяснение обсуждаемого здесь эффекта «с нуля», отбросив теорию двухкомпонентной смеси. Используя компьютерное моделирование, он рассмотрел физические свойства воды в широком диапазоне температур — от 200 до 360 К при нулевом давлении, чтобы в молекулярном масштабе выяснить истинные причины расширения воды при ее охлаждении. Его статья в журнале Physical Review Letters так и называется: Why Does Water Expand When It Cools? («Почему вода при охлаждении расширяется?»).
Изначально автор статьи задался вопросом: что влияет на коэффициент теплового расширения воды? Мацумото считает, что для этого достаточно выяснить влияние всего трех факторов: 1) изменения длины водородных связей между молекулами воды, 2) топологического индекса — числа связей на одну молекулу воды и 3) отклонения величины угла между связями от равновесного значения (углового искажения).
Перед тем как рассказать о результатах, полученных японским физиком, сделаем важные замечания и разъяснения по поводу вышеупомянутых трех факторов. Прежде всего, привычная химическая формула воды H2O соответствует лишь парообразному ее состоянию. В жидкой форме молекулы воды посредством водородной связи объединяются в группы (H2O)x, где x — количество молекул. Наиболее энергетически выгодно объединение из пяти молекул воды (x = 5) с четырьмя водородными связями, в котором связи образуют равновесный, так называемый тетраэдральный угол, равный 109,47 градуса (см. рис. 2).
Проанализировав зависимость длины водородной связи между молекулами воды от температуры, Мацумото пришел к ожидаемому выводу: рост температуры рождает линейное удлинение водородных связей. А это, в свою очередь, приводит к увеличению объема воды, то есть к ее расширению. Сей факт противоречит наблюдаемым результатам, поэтому далее он рассмотрел влияние второго фактора. Как коэффициент теплового расширения зависит от топологического индекса?
Компьютерное моделирование дало следующий результат. При низких температурах наибольший объем воды в процентном отношении занимают кластеры воды, у которых на одну молекулу приходится 4 водородных связи (топологический индекс равен 4). Повышение температуры вызывает уменьшение количества ассоциатов с индексом 4, но при этом начинает возрастать число кластеров с индексами 3 и 5. Проведя численные расчеты, Мацумото обнаружил, что локальный объем кластеров с топологическим индексом 4 с повышением температуры практически не меняется, а изменение суммарного объема ассоциатов с индексами 3 и 5 при любой температуре взаимно компенсирует друг друга. Следовательно, изменение температуры не меняет общий объем воды, а значит, и топологический индекс никакого воздействия на сжатие воды при ее нагревании не оказывает.
Остается выяснить влияние углового искажения водородных связей. И вот здесь начинается самое интересное и важное. Как было сказано выше, молекулы воды стремятся объединиться так, чтобы угол между водородными связями был тетраэдральным. Однако тепловые колебания молекул воды и взаимодействия с другими молекулами, не входящими в кластер, не дают им этого сделать, отклоняя величину угла водородной связи от равновесного значения 109,47 градуса. Чтобы как-то количественно охарактеризовать этот процесс угловой деформации, Мацумото с коллегами, основываясь на своей предыдущей работе Topological building blocks of hydrogen bond network in water, опубликованной в 2007 году в Journal of Chemical Physics, выдвинули гипотезу о существовании в воде трехмерных микроструктур, напоминающих выпуклые полые многогранники. Позднее, в следующих публикациях, такие микроструктуры они назвали витритами (рис. 3). В них вершинами являются молекулы воды, роль ребер играют водородные связи, а угол между водородными связями — это угол между ребрами в витрите.
Согласно теории Мацумото, существует огромное разнообразие форм витритов, которые, как мозаичные элементы, составляют большую часть структуры воды и которые при этом равномерно заполняют весь ее объем.
Молекулы воды стремятся создать в витритах тетраэдральные углы, поскольку витриты должны обладать минимально возможной энергией. Однако из-за тепловых движений и локальных взаимодействий с другими витритами некоторые микроструктуры не обладают геометрией с тетраэдральными углами (или углами, близкими к этому значению). Они принимают такие структурно неравновесные конфигурации (не являющиеся для них самыми выгодными с энергетической точки зрения), которые позволяют всему «семейству» витритов в целом получить наименьшее значение энергии среди возможных. Такие витриты, то есть витриты, которые как бы приносят себя в жертву «общим энергетическим интересам», называются фрустрированными. Если у нефрустрированных витритов объем полости максимален при данной температуре, то фрустрированные витриты, напротив, обладают минимально возможным объемом.
Компьютерное моделирование, проведенное Мацумото, показало, что средний объем полостей витритов с ростом температуры линейным образом уменьшается. При этом фрустрированные витриты значительно уменьшают свой объем, тогда как объем полости нефрустрированных витритов почти не меняется.
Итак, сжатие воды при увеличении температуры вызвано двумя конкурирующими эффектами — удлинением водородных связей, которое приводит к увеличению объема воды, и уменьшением объема полостей фрустрированных витритов. На температурном отрезке от от 0 до 4°C последнее явление, как показали расчеты, преобладает, что в итоге и приводит к наблюдаемому сжатию воды при повышении температуры.
Осталось дождаться экспериментального подтверждения существования витритов и такого их поведения. Но это, увы, очень непростая задача.
Источник: Masakazu Matsumoto. Why Does Water Expand When It Cools? // Phys. Rev. Lett. 103, 017801 (2009).
5 аномальных фактов о воде
Перед вами пять наиболее интересных фактов о воде.
1. Горячая вода замерзает быстрее холодной
Почему же так происходит?
В 1963 году один танзанский студент по имени Эрасто Б. Мпемба (Erasto B. Mpemba) замораживая приготовленную смесь для мороженого, заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Когда юноша поделился своим открытием с учителем физики, тот лишь посмеялся над ним.
К счастью, ученик оказался настойчивым и убедил учителя провести эксперимент, который и подтвердил его открытие: в определенных условиях горячая вода действительно замерзает быстрее холодной.
Теперь этот феномен горячей воды, замерзающей быстрее холодной, носит название «эффект Мпемба». Правда, за долго до него это уникальное свойство воды было отмечено Аристотелем, Фрэнсисом Бэконом и Рене Декартом.
Ученые так до конца и не понимают природу этого явления, объясняя его либо разницей в переохлаждении, испарении, образовании льда, конвекции, либо воздействием разжиженных газов на горячую и холодную воду.
2. Сверхохлаждение и «мгновенное» замерзание
Все знают, что вода всегда превращается в лед при охлаждении до 0 °C … за исключением некоторых случаев! Таким случаем, например, является сверхохлаждение, которое представляет собой свойство очень чистой воды оставаться жидкой, даже будучи охлажденной до температуры ниже точки замерзания.
Это явление становится возможным благодаря тому, что окружающая среда не содержит центров или ядер кристаллизации, которые могли бы спровоцировать образование кристаллов льда. И поэтому вода остается в жидкой форме, даже будучи охлажденной до температуры ниже нуля градусов по Цельсию.
Процесс кристаллизации может быть спровоцирован, например, пузырьками газа, примесями (загрязнениями), неровной поверхностью емкости. Без них вода будет оставаться в жидком состоянии. Когда процесс кристаллизации запускается, можно наблюдать, как сверхохлажденная вода моментально превращается в лед.
Заметьте, что «сверхнагретая» вода также остается жидкой, даже будучи нагретой до температуры выше точки закипания.
3. «Стеклянная» вода
Не задумываясь, назовите, сколько различных состояний есть у воды? Если вы ответили три: твердое, жидкое, газообразное, то вы ошиблись. Ученые выделяют как минимум 5 различных состояний воды в жидком виде и 14 состояний в замерзшем виде.
Что же произойдет при дальнейшем понижении температуры?
4. Квантовые свойства воды
На молекулярном уровне вода удивляет ещё больше. В 1995 году проводимый учеными эксперимент по рассеянию нейтронов дал неожиданный результат: физики обнаружили, что нейтроны, направленные на молекулы воды, «видят» на 25% меньше протонов водорода, чем ожидалось.
5. Есть ли у воды память?
Альтернативная официальной медицине гомеопатия утверждает, что разбавленный раствор лекарственного препарата может оказывать лечебный эффект на организм, даже если коэффициент разбавления настолько велик, что в растворе уже не осталось ничего, кроме молекул воды.
Сторонники гомеопатии объясняют этот парадокс концепцией под названием «память воды», согласно которой вода на молекулярном уровне обладает «памятью» о веществе, некогда в ней растворенном и сохраняет свойства раствора первоначальной концентрации после того, как в нём не остается ни одной молекулы ингредиента.
Международная группа ученых во главе с профессором Мэдлин Эннис (Madeleine Ennis) из Королевского университета в Белфасте (Queen’s University of Belfast), критиковавшая принципы гомеопатии, в 2002 году провела эксперимент, чтобы раз и навсегда опровергнуть эту концепцию.
Результат оказался обратным. После чего, ученые заявили, что им удалось доказать реальность эффекта «памяти воды». Однако опыты, проведенные под наблюдением независимых экспертов, результатов не принесли. Споры о существовании феномена «памяти воды» продолжаются.
Вода обладает множеством других необычных свойств, о которых мы не рассказали в этой статье. Например, плотность воды меняется в зависимости от температуры (плотность льда меньше плотности воды); вода обладает довольно большой величиной поверхностного натяжения; в жидком состоянии вода представляет собой сложную и динамически меняющуюся сеть из водных кластеров, и именно поведение кластеров влияет на структуру воды и т.д.
Если до бесконечности сжимать воду, она сожмется или перестанет быть водой?
Ну, если до бесконечности, то сначала сомнете атомные ядра и вгоните туда электроны оболочек. Получиться нейтронное вещество. Если сжимать дальше, получите кварковую плазму и так далее.
Но реально, человечество пока не умеет достигать таких больших давлений в нужных масштабах.
А из того что достижимо, хватает для получения только «горячего льда».
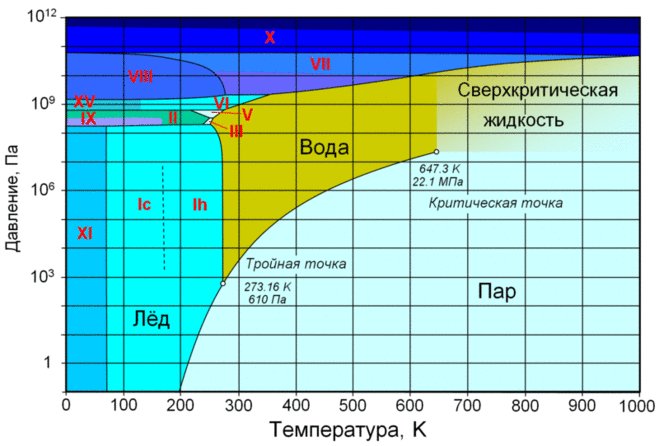
Для того, чтобы узнать, а что будет с веществом при таком-то давлении и температуре, существуют фазовые диаграммы состояний вещества. Вот для воды эта диаграмма выглядит так.
(Не забудьте, что температура указана в градусах Кельвина, а не Цельсия!)
Фазовая диаграмма состояния воды. Римскими цифрами обозначены модификации льда.
И если давить на неполную пластиковую бутылку с водой, но мятую, то под давлением воды бутылка расправится, ибо давление на воду распространяется с одинаковой силой во все стороны. Именно на этом законе физики и работают гидравлические прессы.
Так что сжать воду невозможно, её строение можно только поломать, то есть создать новое вещество если изобрести этот чудо-юдо пресс.
«До бесконечности» ничего совершать невозможно. Даже Земля не может вращаться вокруг Солнца до бесконечности. А само Солнце не может до бесконечности светить. А что будет с водой, если в замкнутом объеме на нее оказывать давление? Она начнет сжиматься, как и все тела (конечно. сжимаемость воды намного меньше, чем, например, сжимаемость газов). Посмотрим на диаграмму состояния воды (вернее, вещества Н2О), которую привел В.А.Топоров. Начнем с комнатной температуры (300 К) и атмосферного давления (1000 Па) и будем при этой температуре увеличивать давление. Вода начнет понемногу сжиматься (коэффициент сжимаемости воды и других жидкостей и твердых тел можно посмотреть в таблице http://infotables.ru /fizika/299-szhimaemo st-elementov-i-zhidko stej-tablitsa
Речь, очевидно, идёт о бутилированной воде, обычно производитель приводит, действительно, такие показатели. Я думаю, что это неплохой маркетинговый ход, с одной стороны, а с другой, всё-таки некоторая информация для покупателя. Есть заболевания ЖКТ, которые требуют от питания большого внимания, осторожности даже при выборе питьевой воды, степени очистки и содержании ионов.
Всегда покупатель ведётся на то, если указаны, например, ионы серебра, считается, что это гарантия чистоты. Я тоже с этим соглашусь.
Потом, у каждого свой вкус воды, я покупаю из конкретной скважины, из своего региона. Долгое время хранить в пластмассовой таре даже воду опасно, растворятся вредные ионы из пластмассы.
Присутствие ионов калия, кальция, хлора, магния это очень хорошее облагораживание воды, нам нужны эти микроэлементы ежедневно, в минимальном объёме.
Глицирин прекрасно смешивается с водой. Он даже поглощает влагу из воздуха (если в помещении есть влажность). Косметические средства на основе глицирина увлажняют кожу лица, рук,придает эластичность, но не забываем способность вытягивать воду, поэтому крем наносить только во влажных помещениях, например в ванной комнате.
Первый случай. Лед плавает в воде при нулевой температуре, система очень хорошо термоизолирована, в сосуде плотная крышка, вода не испаряется. Такое положение называется безразличным равновесием. То есть лед не тает, вода не замерзает.
Третий случай. Лед и вода в кастрюле находятся в условиях, когда тепловая энергия передается от кастрюли, воды и льда наружу. Например, кастрюлю выставили зимой на холод (температура ниже нуля) или поставили в морозильную камеру. В этом случае вода будет замерзать, но если содержимое перемешивать, то температура еще не замерзшей воды, как и льда, будет по-прежнему нулевой. После замерзания всей воды в кастрюле температура льда в ней начнет понижаться, пока не станет равной температуре окружающего воздуха.
В литиевой батарейке реакция идет «в одну сторону». То есть, один элемент (литий) вступает в «не обратимую реакцию» с другим элементом. Приложение к такой батарейке внешнего напряжение или пропускание через неё тока, не приведет к восстановлению элементов в их исходное состояние. А даже может привести к взрыву.
А вот литиевый (вообще, любой) аккумулятор, как раз сконструирован таким образом, что при пропускании через него тока, прореагировавшие до этого элементы, восстанавливаются в исходное состояние (почти!) и снова готовы к реакции и генерированию тока.
Вообще концентрацию, «крепость» водки производят с помощью спиртометра или ареометра..
Приборчик опускают в раствор и по шкале смотрят..
Принцип основан на законе Архимеда..
Если нет такого прибора, то можно налить в мерную посуду например литр и взвесить..
А потом взвесить мерную посуду пустую..
Потом решаем систему линейных алгебраических уравнений:
r1,r2- плотности спирта, воды соответственно
Находим отсюда объём спирта V1..
Отношение V1/V* 100% и есть объёмная концентрация спирта..
Этот способ может дать очень точные показания, если взять химическую мерную посуду и точные весы..