Как называется процесс образования катиона
Катион, формула катиона, образование катиона
Катион, формула катиона, образование катиона.
Катион – положительно заряженный ион, это ион с меньшим количеством электронов, чем протоны, придающие ему положительный заряд.
Катион, формула катиона, образование катиона:
Катион – положительно заряженный ион. Название «катион» происходит от греческого слова «καθιών»: нисходящий, идущий вниз. Термин введён Майклом Фарадеем, в 1834 году.
Катион – это ион с меньшим количеством электронов, чем протоны, придающие ему положительный заряд.
Соли всегда состоят из катионов и анионов.
Катион: образование, различия с анионом и примеры
Содержание:
А катион это химическое вещество, имеющее положительный заряд. Вместе с анионом он образует два типа существующих ионов. Его заряд является результатом нехватки электронов в атоме, что заставляет протоны в ядре проявлять большее притяжение. На каждый электрон, который теряет нейтральный атом, положительный заряд увеличивается на одну единицу.
Если атом теряет электрон, и поэтому число протонов больше единицы, то его положительный заряд будет +1; если вы потеряете два электрона, заряд будет +2 и так далее.Когда катион имеет заряд +1, он называется одновалентным; с другой стороны, если указанный заряд больше +1, катион считается поливалентным.
Как образуется катион?
Было упомянуто, что когда атом теряет электрон, большее количество протонов в нем по сравнению с электронами создает силу притяжения, которая преобразуется в положительный заряд. Но как может произойти потеря электрона? Ответ зависит от превращения, происходящего в химических реакциях.
Следует отметить, что наличие положительно заряженного атома не обязательно означает образование катиона. Чтобы его можно было рассматривать как таковое, не должно быть атома с отрицательным формальным зарядом, который нейтрализует его. В противном случае внутри одного и того же соединения было бы притяжение и отталкивание, и оно было бы нейтральным.
Официальные загрузки и другие ссылки
Электроотрицательные атомы притягивают к себе электроны из своих ковалентных связей. Даже если электроны разделены поровну, наступит момент, когда у них будет частично меньше электронов, чем в их базовой конфигурации; это его свободные атомы, не связанные с другими элементами.
Тогда эти электроотрицательные атомы начнут испытывать недостаток электронов, и вместе с этим протоны их ядер будут проявлять большую силу притяжения; рождается положительный формальный заряд. Если есть только один положительный формальный заряд, соединение будет проявлять общий положительный ионный заряд; таким образом рождается катион.
Атом кислорода катиона H3ИЛИ + Это верный пример вышесказанного. Имея три связи O-H, на одну больше, чем в молекуле воды (H-O-H), он испытывает потерю электрона из своего базового состояния. Формальные расчеты расходов позволяют определить, когда это произойдет.
Окисление
Металлы в первую очередь являются катионообразователями. Однако не все из них могут образовывать ковалентные связи (или, по крайней мере, чисто ковалентные). Вместо этого они теряют электроны, чтобы установить ионные связи: положительный заряд притягивает отрицательный, удерживаемый физическими силами.
Отличия от аниона
Различия между катионом и анионом перечислены ниже:
-Катион в целом меньше, чем анион. На изображении выше показано, как атомный радиус Mg уменьшается за счет потери двух электронов и превращения Mg в катион. 2+ ; с анионами происходит обратное: они становятся более объемными.
-У него больше протонов, чем электронов, а у аниона больше электронов, чем протонов.
— Чем меньше размер, тем выше плотность заряда и, следовательно, большая поляризующая сила; то есть деформирует электронные облака соседних атомов.
-Катион движется в том же направлении, что и приложенное электрическое поле, а анион движется в противоположном направлении.
Примеры наиболее распространенных катионов
Одноатомный
Одноатомные катионы происходят в основном из металлов (за некоторыми исключениями, такими как H + ). В остальном крайне редко можно рассматривать катион, полученный из неметаллического элемента.
Будет видно, что многие из них двух- или поливалентны, и что величина их зарядов согласуется с числом их групп в периодической таблице.
Эти двухвалентные катионы являются производными соответствующих металлов, принадлежащих к группе 2: щелочноземельных металлов.
Трехвалентные катионы группы бора.
До сих пор эти примеры характеризовались как имеющие одну валентность или заряд. Другие катионы проявляют более одной валентной или положительной степени окисления:
А другие металлы, такие как марганец, могут иметь еще больше валентностей:
Чем выше заряд, тем меньше и сильнее поляризуется катион.
Многоатомный
Не вдаваясь в органическую химию, есть неорганические и многоатомные катионы, которые очень часто встречаются в повседневной жизни; такие как:
-ЧАС3ИЛИ + (гидроксоний, уже упоминалось).
-НЕТ2 + (Нитроний, присутствующий в процессах нитрования).
Ссылки
10 лучших гериатрических резиденций в Мурсии
Большая Энциклопедия Нефти и Газа
Образование катиона из изобутилена под действием ионизирующего излучения было подтверждено с помощью масс-спектрометрии. [1]
Образование катиона Mg2 в растворах этилового эфира нужно считать в высшей степени мало вероятным, ввиду низкой диэлектрической постоянной растворителя. [2]
Образование катионов Sb3 и SbS мало вероятно, поскольку сульфид сурьмы не диссоциирует в воде. [5]
Образование катиона III обычно является самой медленной стадией, определяющей скорость всего процесса как для прямой, так и для обратной реакции. Ацетализация п гидролиз ацеталя протекают в этих случаях мономолекулярно ( см. также стр. [6]
Образование бициклобутониевого катиона происходит за счет делокализации сг-связей циклов или я-связи, не сопряженной с электронодефицитным центром. В этом катионе три атома уг лерода имеют дефицит в электронной плотности и по каждом из них может происходить взаимодействие с противоионом; еслр анион реагирует с С1, получается замещенный циклобутан, есл. [10]
Образование пентадиенового катиона требует малой затраты энергии, так как энергия сопряжения этой сопряженной системы ( равная, согласно некоторым квантово-механическим расчетам, 26 ккал / молъ) компенсирует в большой степени потерю энергии сопряжения бензола ( 36 ккал / молъ); таким образом, реакция должна обеспечить только разность этих энергий. В действительности многие реакции замещения ароматического ядра идут со сравнительно малыми энергиями активации. В последнее время стало возможным выделить промежуточные комплексы такого типа в чистом виде, как будет указано ниже. [11]
Образование пентадиенового катиона требует малой затраты энергии, так как энергия сопряжения этой сопряженной системы ( равная, согласно некоторым квантово-механическим расчетам, 26 ккал / моль) компенсирует в большой степени потерю энергии сопряжения бензола ( 36 ккал / молъ), таким образом, реакция должна обеспечить только разность этих энергий. В действительности многие реакции замещения ароматического ядра идут со сравнительно малыми энергиями активации. В последнее время стало возможным выделить промежуточные комплексы такого типа в чистом виде, как будет указано ниже. [13]
Образованию катионов ацилия из галогенангидридов способствуют, в частности, кислоты Льюиса ( см. гл. [15]
Катионы и анионы в химии, таблица растворимости
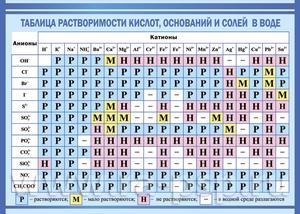
Показатели растворимости в воде
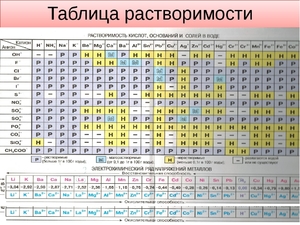
Она помогает при решении химических уравнений, где участвуют ионные реакции. Если результатом будет получение нерастворимого вещества, то реакция возможна. Существует несколько вариантов:
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
Электролиты
Это растворы или сплавы, проводящие электрический ток. Электропроводность их объясняется мобильностью ионов. Электролиты можно поделить на 2 группы:
Теория электролитической растворимости
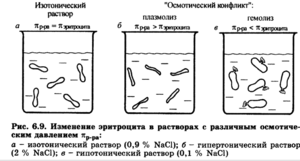
Одновременно с диссоциацией проходит противоположный процесс – соединение ионов в молекулы. Кислоты – это такие электролиты, при распаде которых образуется катион – ион водорода. Основания – анионы – это гидроксид ионы. Щелочи – это основания, которые растворяются в воде. Электролиты, которые способны образовывать и катионы и анионы, называются амфотерными.
Это такая частица, в которой больше протонов или электронов, он будет называться анион или катион, в зависимости от того, чего больше: протонов или электронов. В качестве самостоятельных частиц они встречаются во многих агрегатных состояниях: газах, жидкостях, кристаллах и в плазме. Понятие и название ввёл в обиход Майкл Фарадей в 1834 году. Он изучал воздействие электричества на растворы кислот, щелочей и солей.
Простые ионы несут на себе ядро и электроны. Ядро составляет почти всю атомную массу и состоит из протонов и нейтронов. Количество протонов совпадает с порядковым номером атома в периодической системе и зарядом ядра. Ион не имеет определённых границ из-за волнового движения электронов, поэтому невозможно измерить их размеры.
Отрыв электрона от атома требует, в свою очередь, затрат энергии. Она называется энергия ионизации. Когда присоединяется электрон, происходит выделение энергии.
Катионы
Это частицы, носящие положительный заряд. Могут иметь разную величину заряда, например: Са2+ — двузарядный катион, Na+ — однозарядный катион. Мигрируют к отрицательному катоду в электрическом поле.
Анионы
Это элементы, имеющие отрицательный заряд. А также обладает различным количеством величины зарядов, например, CL- — однозарядный ион, SO42- — двухзарядный ион. Такие элементы входят в состав веществ, обладающих ионной кристаллической решёткой, в поваренной соли и многих органических соединениях.
Химия – наука, где возможно творить практически любые чудеса. Катион вы можете узнать по ссылке.
Как называется процесс образования катиона
Ключевые слова конспекта: Катионы как продукт окисления атомов металлов. Анионы как продукт восстановления атомов неметаллов. Ионная химическая связь. Ионная кристаллическая решётка. Простые и сложные ионы.
Опираясь на знания из курса основной школы, вы, возможно, предложите следующие способы:
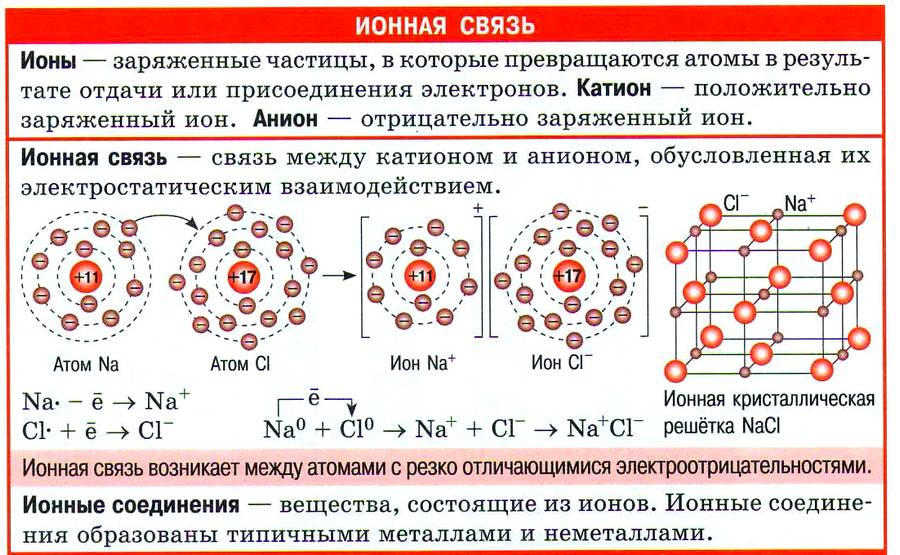
Однако эти процессы имеют далеко идущие последствия. Во–первых, атомы металлов, отдавая электроны (процесс называется окислением), превращаются в положительно заряженные ионы — катионы, а во–вторых, атомы неметаллов, принимая электроны на внешний слой (процесс называется восстановлением), превращаются в отрицательно заряженные ионы — анионы.
Согласно закону Кулона, между катионами и анионами возникают силы электростатического притяжения, которые удерживают эти частицы в ионном кристалле.
Эта связь характерна для соединений, образованных наиболее активными металлами — щелочными и щёлочноземельными, и наиболее активными неметаллами — галогенами и кислородом. Следовательно, из бинарных, или двухэлементных соединений, к ионным относятся оксиды и галогениды металлов IA- и IIА-групп. Эти соединения построены простыми ионами.
Схематично процесс образования ионной связи между атомами кальция и хлора можно отразить следующим образом:
Два разноимённо заряженных иона, связанных силами взаимного притяжения, взаимодействуют с другими противоположно заряженными ионами, образуя таким образом кристаллические соединения. Что они собой представляют?
Ионы, как и другие частицы, в твёрдом кристалле занимают строго определённое положение в пространстве. Если их соединить воображаемыми линиями, получится совокупность ячеек правильной геометрической формы, называемая кристаллической решёткой. Точки, в которых расположены частицы вещества (в нашем случае ионы), называют узлами кристаллической решётки.
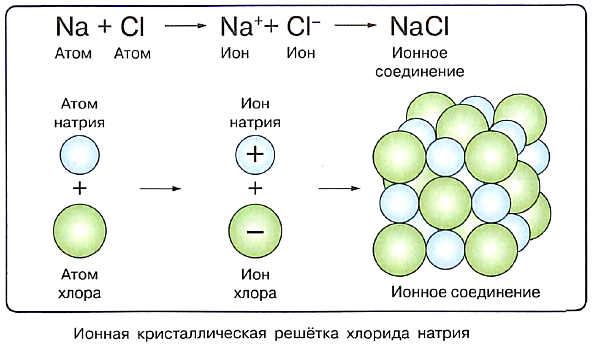
На рисунке представлена модель кристаллической решётки другого ионного соединения — хлорида натрия NaCl. В нём каждый катион натрия окружён шестью хлорид-анионами. Те, в свою очередь, окружены каждый шестью катионами натрия.
Ионы в узлах кристаллической решётки могут колебаться, но перемещаться им мешают другие ионы. Силы взаимного притяжения ионов достаточно велики, поэтому при обычных условиях вещества ионного строения имеют твёрдое агрегатное состояние, высокую температуру плавления, они нелетучие, а потому без запаха. Некоторые из таких веществ хорошо растворимы в воде (гидроксиды щелочных и щёлочноземельных металлов, соли).
Ионные кристаллы хрупкие, поскольку при смещении слоёв одинаково заряженные ионы сближаются друг с другом, что приводит к их взаимному отталкиванию.
При сильном нагревании колебание ионов увеличивается настолько, что порядок нарушается и кристалл плавится. Из каких частиц будет состоять полученная жидкость? Очевидно, из тех, которые были в узлах кристаллической решётки, т. е. из ионов.
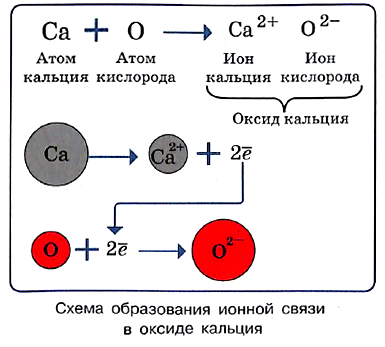
На рисунке показана схема образования ионной связи в оксиде кальция СаО, хорошо известного под названием «негашёная известь».
Поскольку соединения с ионной связью относятся к веществам немолекулярного строения, более точным термином, отражающим их состав, является термин «формульная единица», а не «молекулярная формула». Однако в силу традиций последнее название часто употребляется и в отношении ионных соединений.
Ионную связь можно рассматривать как крайнюю степень полярности ковалентных связей. Даже в тех соединениях, которые считаются абсолютно ионными, например в хлориде натрия, отсутствуют ионы с целочисленными значениями зарядов (+1 и –1). Действительный заряд на катионе натрия и хлорид–анионе соответственно равен +0,8 и –0,8.
Не является абсолютно истинным и утверждение о том, что ионная связь возникает между элементами с противоположными свойствами — между активными металлами и неметаллами. Имеются ионные соединения, построенные только из неметаллов. К ним, например, можно отнести соли аммония (сульфат аммония, хлорид аммония и др.), а также соли органических оснований — аминов (хлорид метиаламмония, нитрат этиламмония и др.).
Теорию ионной связи предложил немецкий учёный Вальтер Коссель.
Конспект урока по химии «Ионная химическая связь и ионные кристаллические решётки «. В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие: