дронедарон нельзя использовать у пациентов с
Дронедарон
Фармдействие
Дронедарон обладает электрофизиологическими свойствами, характерными для всех четырех классов антиаритмиков по классификации Воген-Вильямса. Дронедарон является блокатором нескольких ионных каналов, ингибирующим калиевые токи (эффект антиаритмиков III класса), включая выходящий калиевый ток задержанного выпрямления, активируемый ацетилхолином (IK(Ach), сверхбыстрый выходящий калиевый ток задержанного выпрямления (IKur), быстрый выходящий калиевый ток задержанного выпрямления (IКг) и медленный выходящий калиевый ток задержанного выпрямления (IKs). За счет этого происходит удлинение потенциала действия и рефрактерного периода клеток миокарда. Дронедарон также ингибирует натриевые токи (эффект антиаритмиков IB класса) и кальциевые токи (эффект антиаритмиков IV класса). Дронедарон является неконкурентным антагонистом адренергической активности (эффект антиаритмиков II класса).
Дронедарон обладает сосудорасширяющим действием, связанным с активацией синтеза оксида азота, и более выраженным в коронарных, чем в периферических артериях.
Дронедарон оказывает непрямое антиадренергическое действие, снижает опосредуемую через альфа-адренергические рецепторы реакцию артериального давления на эпинефрин (адреналин) и опосредуемую через бета1- и бета2-адренергические рецепторы реакции на изопротеренол.
У пациентов, получающих дронедарон с целью поддержания синусового ритма, в случае возникновения рецидива мерцательной аритмии последний протекает с меньшей частотой желудочковых сокращений, чем таковой у пациентов, не получающих дронедарон.
Фармакокинетика:
Всасывание. При приеме внутрь одновременно с пищей дронедарон хорошо абсорбируется (не менее 70 %). Однако в связи с пресистемным метаболизмом при первом прохождении через печень абсолютная биодоступность дронедарона (принятого с пищей) составляет 15 %. Одновременный прием пищи увеличивает биодоступность дронедарона в 2-4 раза. После приема внутрь с пищей Cmaxдронедарона и его основного активного метаболита (N-дебутилметаболита) в плазме достигается в течение 3-6 ч. При курсовом приеме по 400 мг 2 раза в день CSS в плазме достигается за 4-8 дней лечения, и среднее значение коэффициента накопления дронедарона составляет 2,6-4,5. Среднее значение Cmax дронедарона в равновесном состоянии составляет 84-147 нг/мл, концентрация основного N-дебутилметаболита имеет такие же средние значения. При увеличении доз дронедарона значения Cmax и AUC дронедарона и его N-дебутилметаболита также повышаются, причем их повышение незначительно опережает простую пропорциональность дозе: увеличение дозы в 2 раза приводит к увеличению соответствующих фармакокинетических показателей в 2,5-3 раза.
Распределение. Связь с белками плазмы крови дронедарона и его N-дебутилметаболита in vitro превышает 98 % и является ненасыщаемой. Оба вещества связываются преимущественно с альбумином. После внутривенного введения VSS колеблется от 1200 до 1400 л.
Метаболизм. Дронедарон интенсивно метаболизируется преимущественно с помощью изофермента CYP3A4. Основной путь метаболизма состоит из N-дебутилирования с образованием основного активного метаболита, присутствующего в крови с его последующим окислением, окислительным дезаминированием с образованием неактивного метаболита пропионовой кислоты с ее дальнейшим окислением. Моноаминооксидазы частично вносят свой вклад в метаболизм активного метаболита дронедарона. Фармакодинамическая активность N-дебутилметаболита в 3-10 раз меньше фармакодинамической активности дронедарона.
Показания
Мерцание предсердий или трепетание предсердий в анамнезе или в настоящее время (для снижения риска госпитализации по поводу сердечно-сосудистых заболеваний).
Противопоказания
— атриовентрикулярная блокада II или III степени или синдром слабости синусового узла (за исключением применения у пациентов с функционирующим искусственным водителем ритма);
— выраженная брадикардия (частота сердечных сокращений менее 50 ударов в минуту);
— продолжительность интервала QTc ≥ 500 мс;
— хроническая сердечная недостаточность IV функционального класса по классификации NYHA или хроническая сердечная недостаточность III функционального класса по классификации NYHA с недавней декомпенсацией, потребовавшей госпитализации или направления в специализированную клинику;
— одновременный прием сильных ингибиторов изофермента CYP3A4, таких как кетоконазол, итраконазол, вориконазол, телитромицин, кларитромицин, нефазодон и ритонавир;
— одновременный прием препаратов, способных вызывать развитие пароксизмальных тахикардий, включая полиморфную желудочковую тахикардию типа «пируэт»: фенотиазинов, цизаприда, бепридила, трициклических антидепрессантов, терфенадина и некоторых макролидов для приема внутрь, антиаритмиков I и III классов;
— тяжелая печеночная недостаточность;
— тяжелая почечная недостаточность (клиренс креатинина менее 30 мл/мин);
— беременность и период лактации;
— наследственная непереносимость галактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция (из-за наличия в составе препарата лактозы в качестве вспомогательного вещества);
— детский возраст до 18 лет (отсутствие клинического опыта применения дронедарона);
— повышенная чувствительность к дронедарону или вспомогательным веществам препарата.
Дозирование
Внутрь, во время еды (во время завтрака и ужина), запивая 1/2 стакана воды. Лечение может начинаться амбулаторно. Перед началом приема следует прекратить лечение антиаритмическими средствами (такими как флекаинид, пропафенон, хинидин, дизопирамид, дофетилид, амиодарон и соталол).
Дети и подростки. Так как безопасность и эффективность у пациентов моложе 18 лет не установлена, применение дронедарона у этих пациентов не рекомендуется.
Пациенты пожилого возраста. Эффективность и безопасность применения препарата у пациентов пожилого возраста не отличается от таковых у пациентов более молодого возраста, и коррекции дозы у этой категории пациентов не требуется.
Побочные эффекты
Если любые из указанных в инструкции побочных эффектов усугубляются, или пациент заметил любые другие побочные эффекты, не указанные в инструкции, следует сообщить об этом врачу.
Взаимодействие
Прием 300 мл грейпфрутового сока 3 раза в день приводил к трехкратному увеличению системной экспозиции дронедарона. Поэтому пациентам следует отказаться от приема грейпфрутового сока во всех его видах во время приема препарата.
Противопоказано одновременное с дронедароном применение вориконазола (сильный ингибитор изофермента CYP3A4).
Дронедарон (400 мг 2 раза в день) увеличивал системную экспозицию дигоксина в 2,5 раза за счет ингибирования транспортера Р-гликопротеина. Кроме того, дигоксин обладает потенциальной возможностью фармакодинамического взаимодействия с дронедароном. В клинических исследованиях в случаях, когда дронедарон принимался совместно с дигоксином, наблюдалось увеличение концентрации дигоксина в сыворотке крови и/или нежелательных явлений со стороны пищеварительной системы. Вследствие фармакокинетического и возможного фармакодинамического взаимодействия следует соблюдать осторожность, если дигоксин применяется совместно с дронедароном. Если продолжается лечение дигоксином, то его дозу следует уменьшить в 2 раза, проводить регулярное определение концентрации дигоксина в сыворотке крови и контроль состояния пациентов на предмет выявления признаков гликозидной интоксикации.
Дронедарон ингибирует Р-гликопротеин и, возможно, его взаимодействие с доксорубицином (субстрат Р-гликопротеина), приводящее к повышению концентрации доксорубицина в сыворотке крови и усилению его фармакодинамических и токсических побочных эффектов.
Не рекомендуется одновременное применение дронедарона и лекарственных средств, содержащих зверобой продырявленный (индукторы изофермента CYP3A4), так как они снижают системную экспозицию дронедарона.
Противопоказано одновременное с дронедароном применение итраконазола и/или кларитромицина (сильные ингибиторы изофермента CYP3A4).
Не рекомендуется одновременное применение дронедарона и карбамазепина (индуктор изофермента CYP3A4), так как карбамазепин снижает системную экспозицию дронедарона.
Курсовой прием 200 мг кетоконазола (сильный ингибитор изофермента CYP3A4) в сутки вызывал 17-кратное увеличение системной экспозиции дронедарона. Поэтому противопоказано одновременное с дронедароном применение кетоконазола.
Пасиреотид следует с осторожностью применять одновременно с дронедароном, способным удлинять интервал QT.
Противопоказано одновременное с дронедароном применение ритонавира (сильный ингибитор изофермента CYP3A4).
Рифампицин (индуктор изофермента CYP3A4) (600 мг 1 раз в день) снижал системную экспозицию дронедарона в 5 раз, не оказывая при этом значительное воздействие на системную экспозицию его активного метаболита. Поэтому не рекомендуется одновременное применение дронедарона и рифампицина.
Дронедарон может повышать плазменную концентрацию сиролимуса и такролимуса. При совместном применении с дронедароном рекомендованы регулярный контроль плазменной концентрации сиролимуса и такролимуса и соответствующая коррекция дозы.
Дронедарон ингибирует Р-гликопротеин и, возможно, его взаимодействие с талинололом (субстрат Р-гликопротеина), приводящее к повышению концентрации талинолола в сыворотке крови и усилению его фармакодинамических и токсических побочных эффектов.
Терфенадин и цизаприд способны вызывать удлинение интервала QT и/или развитие пароксизмальной тахикардии, включая желудочковую тахикардию типа «пируэт». Одновременный прием совместно с дронедароном противопоказан (имеется потенциальный риск развития проаритмогенного действия).
Дронедарон ингибирует Р-гликопротеин и, возможно, его взаимодействие с фексофенадином (субстрат Р-гликопротеина), приводящее к повышению концентрации фексофенадина в сыворотке крови и усилению его фармакодинамических и токсических побочных эффектов.
Не рекомендуется одновременное применение дронедарона и фенитоина, фенобарбитала (индукторы изофермента CYP3A4), так как они снижают системную экспозицию дронедарона.
Особые указания
С осторожностью:
При гипокалиемии, гипомагниемии (дефицит калия или магния должен быть обязательно восполнен до начала и во время лечения препаратом; при одновременном приеме ингибиторов ГМГ-КоА-редуктазы (статинов), метаболизирующихся с помощью изофермента CYP3A4, таких как симвастатин, ловастатин, аторвастатин, правастатин.
Применение дронедарона должно быть ограничено пациентами с пароксизмальной и персистирующей фибрилляцией предсердий при наличии у них синусового ритма. При возникновении рецидивов фибрилляции предсердий/трепетания предсердий на фоне постоянного приема дронедарона должен быть либо быстро восстановлен синусовый ритм, и тогда прием препарата может быть продолжен, либо дронедарон должен быть отменен в случае продолжающейся фибрилляции предсердий.
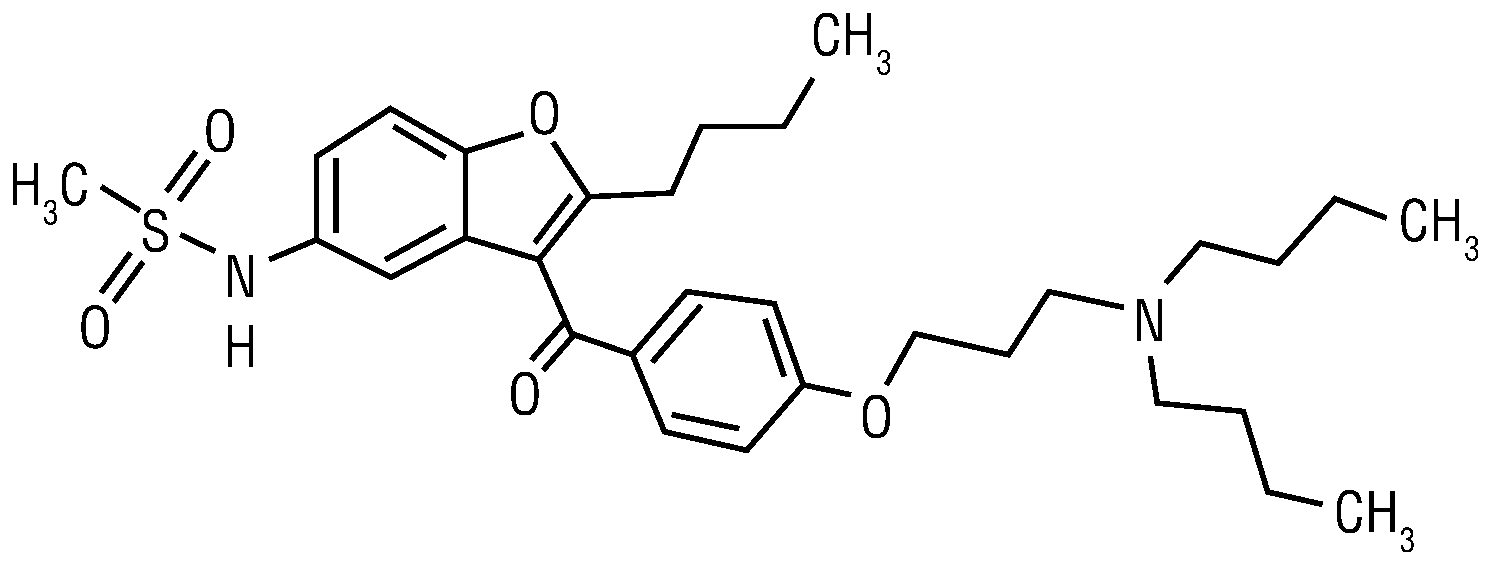
ДРОНЕДАРОН (DRONEDARONE)



NLM: метансульфонамид,N-(2-бутил-3-(4-(3-(дибутиламино)пропокси)-бензоил)-5-бензофуранил)-.
USPDDN: N-(2-бутил-3-(p-(3-(дибутиламино)пропокси)-бензоил)-5-бензофуранил)метансульфонамид.
Mm = 593,2 Да. Белый мелкий порошок, который практически нерастворим в воде и свободно растворим в метиленхлориде и метаноле.
Форма выпуска: таблетки п/о.
Лекарственные препараты содержащие активное вещество ДРОНЕДАРОН
Фармакологические свойства
дронедарон — антиаритмическое средство, показанное для применения у взрослых пациентов в стабильном клиническом состоянии, которые ранее перенесли или в данный момент имеют непостоянную форму фибрилляции предсердий (ФП), с целью предупреждения рецидива ФП или замедления желудочкового ритма.
Дронедарон является мультиканальным блокатором, который ингибирует калиевые каналы (включая IK(Ach), IKur, IKr, IKs), и таким образом удлиняет потенциал действия сердечной мышцы и рефрактерный период (класс III). Он также ингибирует натриевые каналы (класс Ib) и кальциевые каналы (класс IV). Он является неконкурентным антагонистом адренергических рецепторов (класс II).
Дронедарон снижает АД и сократительную способность миокарда, не изменяя фракцию выброса левого желудочка и снижая потребление миокардом кислорода.
Дронедарон обладает сосудорасширяющим действием, которое более выражено относительно коронарных артерий (в связи с активацией сигнального пути оксида азота), по сравнению с периферическими артериями.
Дронедарон оказывает непрямое антиадренергическое действие; снижает α-адренергический ответ со стороны АД на эпинефрин, а также ответ β1— и β2-адренорецепторов на изопротеренол.
После перорального приема с пищей дронедарон всасывается хорошо (по меньшей мере на 70%). Однако ввиду предсистемного первичного метаболизма абсолютная биодоступность дронедарона (который принимается с пищей) составляет 15%. Применение дронедарона во время приема пищи повышает его биодоступность в среднем в 2–4 раза. После перорального приема с пищей Сmax дронедарона и основного циркулирующего активного метаболита (метаболита N-дебутила) в плазме крови достигаются на протяжении 3–6 ч. После повторного приема 400 мг 2 раза в сутки равновесная концентрация достигается на протяжении 4–8 дней лечения и средний коэффициент накопления для дронедарона составляет 2,6–4,5. Стабильная Cmax дронедарона составляет 84–147 нг/мл, и уровень основного метаболита N-дебутила подобен уровню основного соединения. Фармакокинетика дронедарона и его метаболита N-дебутила несущественно изменяется в зависимости от дозы: 2-кратное повышение дозы приводит приблизительно к 2,5–3-кратному повышению Cmax и AUC.
Определенный в лабораторных условиях уровень связывания дронедарона и его метаболита N-дебутила с белками плазмы крови составляет соответственно 99,7 и 98,5% и не обусловливает насыщения. Оба соединения связываются главным образом с альбумином. После в/в применения объем распределения в стабильном состоянии (Vss) колеблется от 1200 до 1400 л.
Дронедарон активно метаболизируется, главным образом CYP 3A4. Основной метаболический путь включает N-дебутилирование с целью образования основного циркулирующего активного метаболита, после чего происходит окисление, окислительное дезаминирование с целью образования неактивного метаболита пропионовой кислоты с дальнейшим окислением и прямым окислением. Метаболит N-дебутил обладает фармакодинамической активностью, однако он в 3–10 раз слабее, чем дронедарон. Этот метаболит принимает участие в фармакологической активности дронедарона у человека.
После перорального применения около 6% определенной дозы выводится с мочой, главным образом в виде метаболитов (неизмененное вещество с мочой не выводится), и 84% — с калом, в основном в виде метаболитов. После в/в применения скорость выведения дронедарона из плазмы крови составляет 130–150 л/ч. Заключительный T½ дронедарона составляет около 25–30 ч, а его метаболита N-дебутила — около 20–25 ч. У пациентов дронедарон и его метаболит полностью выводятся из плазмы крови на протяжении 2 нед с момента прекращения лечения в дозе 400 мг 2 раза в сутки.
Показания ДРОНЕДАРОН
дронедарон показан для применения у взрослых пациентов в стабильном клиническом состоянии, которые ранее перенесли или в данный момент имеют непостоянную форму ФП, с целью предупреждения рецидива ФП или замедления желудочкового ритма. В связи с его профилем безопасности дронедарон следует назначать только после рассмотрения альтернативных подходов к лечению. Дронедарон не следует назначать пациентам с левожелудочковой систолической дисфункцией или пациентам с сердечной недостаточностью, которые имеют эпизоды сердечной недостаточности в анамнезе.
Применение ДРОНЕДАРОН
лечение дронедароном можно начинать в амбулаторных условиях.
Для взрослых рекомендуемая доза составляет 400 мг 2 раза в сутки, утром и вечером во время еды.
Дронедарон не следует запивать грейпфрутовым соком.
В случае пропуска дозы необходимо принять следующую дозу согласно определенной схеме, не следует удваивать дозу.
Перед началом применения дронедарона необходимо прекратить лечение антиаритмическими средствами класса I или III (флекаинид, пропафенон, хинидин, дизопирамид, дофенилид, соталол, амиодарон).
Опыт применения у детей и подростков в возрасте до 18 лет отсутствует, поэтому дронедарон не рекомендуют к применению у этой группы пациентов.
Противопоказания
повышенная чувствительность к дронедарону. AV-блокада II или III степени или синдром слабости синусного узла (за исключением случаев применения одновременно с функционирующим водителем ритма). Брадикардия 500 мс. Тяжелая печеночная недостаточность. Тяжелая почечная недостаточность (клиренс креатинина 1/10), часто (>1/100, 1/1000, 1/10 000, # по Базетту.
*Повышенный уровень креатинина в плазме крови >10% через 5 дней после начала лечения.
# Удлинение интервала Q–Tc, рассчитанное по формуле Базетта (>450 мс у мужчин и >470 мс у женщин).
Особые указания
при применении дронедарона рекомендуется осуществлять тщательный мониторинг путем регулярной оценки функции сердца, печени и легких. В случае рецидива ФП следует рассмотреть целесообразность отмены дронедарона. Во время прохождения курса лечения применение дронедарона требуется прекратить в случае, если у пациента развивается любое из состояний, которые могут привести к возникновению противопоказания. Необходимо проводить мониторинг одновременного применения таких средств, как дигоксин и антикоагулянты.
Пациенты, у которых во время лечения развивается постоянная ФП. Клиническое исследование с участием пациентов с постоянной ФП (при длительности ФП
Лечение фибрилляции предсердий. Исследование «Простор»: новые данные
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
— Следующий доклад. Профессор Миллер Ольга Николаевна. Профессор Миллер представляет новосибирскую школу. Она находится у нас в студии. Доклад посвящен лечению фибрилляции предсердий по материалам Всемирного Конгресса кардиологов. Еще раз будут затронуты результаты исследования «ПРОСТОР».
Ольга Николаевна Миллер, профессор, доктор медицинских наук:
— Добрый день, уважаемые коллеги!
Я хочу с вами обсудить проблему поддержания у больных синусового ритма, с которым мы встречаемся каждый день.
Начну с того, что бороться надо не с самим нарушением сердечного ритма, не с самой фибрилляцией предсердий. Прежде всего, нужно большое внимание обратить на ту причину, которая привела к этому нарушению сердечного ритма.
Вы еще раз видите ту диаграмму, которую я неоднократно показывала. Хочу подчеркнуть, что на первой позиции по причинам фибрилляции предсердий стоит именно артериальная гипертония (АГ). Наша (прежде всего, наша) задача – добиваться целевого уровня артериального давления.
Вторую позицию, вы видите, занимает хроническая сердечная недостаточность со вторым-четвертым функциональным классом.
Что написано в наших российских рекомендациях – это было написано еще в 2007-м году. Одним из основных принципов лечения фибрилляции предсердий считается применение не антиаритмиков, а препаратов, которые блокируют ренин-ангиотензин-альдостероновую систему. Есть тому доказательная база.
Если вы имеете пациента с систолической хронической сердечной недостаточностью, у которого еще нет фибрилляции предсердий, фракция выброса низкая, то назначение ингибиторов и сартанов снижает риск развития фибрилляции предсердий на 30-45%. Хороший, действительно, процент. Мы тем самым можем предупредить развитие этого нарушения сердечного ритма.
Если мы имеем пациента с гипертрофией миокарда левого желудочка на фоне гипертонической болезни, те же самые лекарственные препараты снижают риск фибрилляции предсердий на 25%.
Что же касается статинов, здесь тоже большая доказательная база. Если мы назначаем до хирургического вмешательства эту группу лекарственных препаратов, то они достоверно уменьшают риск развития послеоперационной фибрилляции предсердий на 32%.
Давайте посмотрим, какими же лекарственными препаратами мы можем восстановить синусовый ритм. Это вам, конечно, известно.
Мы тоже понимаем, что восстановить синусовый ритм практически не представляет никаких проблем, если длительность фибрилляции предсердий до 48-ми часов. Даже говорится о том, что в большинстве случаев пароксизмальная форма обрывается самостоятельно, без вмешательства лекарственных препаратов, в течение 24-х часов.
На фармацевтическом рынке всего 2 лекарственных средства: «Амиодарон» («Amiodarone») и «Пропафенон» («Propafenone»). «Амиодарон» вводится, еще раз напомню, 5 мг на килограмм массы тела. Подчеркивается (что в европейских, что в наших российских рекомендациях), что нужно вводить его внутривенно капельно в течение одного часа.
«Пропафенон» существует в таблетированной форме. Чаще мы пользуется «Пропанормом» («Propanorm»). Это так называемая стратегия «таблетка в кармане», когда мы однократно можем воспользоваться дозой 450 или 600 мг.
Если мы посмотрим на мета-анализ 9-ти клинических исследований по эффективности антиаритмического препарата первого класса С и «Амиодарона». Вы видите, что здесь в 70% случаев все-таки использовался «Пропафенон».
На что хочу обратить внимание в этом графике, который перед вами. Дело в том, что в первые 2-3-5 часов эффективность препаратов 1С класса опережает «Амиодарон». Практически в два раза. Только к 24-му часу процент восстановления синусового ритма на фоне «Амиодарона» и препаратов 1С класса практически одинаков.
Но дальше очень большая проблема, которой мы как-то не уделяем должного внимания и очень часто допускаем ошибки. Если пациент с некупированным эпизодом фибрилляции предсердий доставлен в приемный покой, и длительность фибрилляции предсердий менее двух сеток (обратите внимание еще раз на эту цифру: 48 часов), то пациент по правилам должен быть госпитализирован в блок интенсивной терапии для проведения электрической кардиоверсии.
Как только фибрилляция предсердий за 48 часов выходит, здесь абсолютно меняется тактика ведения этих пациентов. Если все-таки еще двое суток не прошло с момента эпизода мерцательной аритмии, непосредственно нужно восстановить синусовый ритм с помощью электрической кардиоверсии, пока не произошло образование тромбов.
С этой целью вводится нефракционированный гепарин. Он вводится под контролем активированного частичного тромбопластинового времени. Параллельно с нефракционированным гепарином может быть назначен либо антагонист витамина К («Варфарин» («Warfarin»), либо «Дабигатран» («Прадакса» («Pradaxa»).
Далее тактика ведения пациента с фибрилляцией предсердий подразумевает не контроль частоты сердечных сокращений (ЧCC) или удержание синусового ритма. Обратите внимание на эту схему, которая есть в наших российских рекомендациях. Надо оценить риск инсульта. Но это сегодня не моя задача.
Мы сегодня обсудим, каким же препаратом лучше всего удерживать синусовый ритм. Это один из главных вопросов, которые задают врачи друг другу и кардиологам-аритмологам.
Если мы посмотрим, каким препаратам, мы увидим, что за каждым лекарственным средством стоит класс рекомендаций А и очень высокий уровень доказательств. Это «Амиодарон», это «Пропафенон», это «Соталол» («Sotalol»).
Но в наших же российских рекомендациях четко написано: учитывая тактический профиль «Амиодарона», он может применяться в случаях, когда другие рекомендованные препараты неэффективны или противопоказаны.
Почему? Общая частота нежелательных эффектов на фоне «Амиодарона» составляет от 17-ти до 70%. У «Амиодарона» самый низкий проаритмогенный эффект, зато самое высокой органотоксичное действие.
В частности, новая информация по «Амиодарону» получена уже в 2012-м году. Пишется о том в этом документе, что зарегистрированы новые случаи развития DRESS-синдрома. Это касается возникновения лихорадки. Сыпь, эозинофилия, аденопатия, амиодарон-ассоциированный гепатит, интерстициальная нефропатия. А также то, о чем мы знали – легочный фиброз. Самое неприятное – со смертельными исходами.
Совет FDA принял решение о внесении новых предостережений в инструкцию по медицинскому применению «Амиодарона». А Центр экспертизы безопасности лекарственных препаратов Российской Федерации просит на сегодняшний день информировать обо всех серьезных нежелательных явлениях, связанных с применением «Амиодарона».
На фармацевтическом рынке все меньше и меньше появляется антиаритмических препаратов. Казалось бы, мы очень долго ждали нового лекарственного препарата – речь идет о «Дронедароне» («Dronedarone»). Это «Амиодарон» без йода.
По крайней мере, на 2009-й год по поводу «Дронедарона», который является антиаритмиком 3-го класса, была информация. Причем Пицини (Piccini) писал об этом: «Наш анализ показал, что эффективность «Дронедарона» не отличается от плацебо в профилактике рецидивов фибрилляции предсердий».
Но это еще не все. Дело в том, что убрав две молекулы йода, оказалось, что «Дронедарон» вообще не способен как-то реагировать на желудочковые нарушения сердечного ритма.
Но давайте вернемся к фибрилляции предсердий. Тогда, в 2009-м году, была информация, что в отличие от «Амиодарона» у него существенно меньше побочных эффектов.
Однако вы знаете последние результаты исследования «PALLAS», когда «Дронедарон» применялся у пациентов с постоянной формой фибрилляции предсердий. Это исследование «PALLAS» 28-го октября 2011-го года было досрочно остановлено. По какой причине? Практически по всем позициям (вы сейчас видите на диаграмме) «Дронедарон», конечно же, проиграл группе плацебо.
В два раза практически по всем этим позициям, которые представлены на диаграмме, смертность была выше. По ишемическому инсульту, по системным тромбоэмболиям. По смертности, по незапрогнозированным декомпенсациям кровообращения, по инсульту и госпитализациям по поводу хронической сердечной недостаточности. Еще один препарат выбыл из нашего арсенала.
Но мы всегда задаем себе вопрос: можно ли применять какие-либо другие антиаритмические препараты, например, при той же самой хронической сердечной недостаточности, но низкого функционального класса. В частности, речь идет о препаратах опять 1С класса.
Мы очень часто в кулуарах, между собой, в ординаторских обсуждаем вопросы. Какие вопросы конкретно. Действительно, мы слишком часто манипулируем таким неоднозначным понятием, как органическое заболевание сердца.
Что мы подразумеваем под органическим заболеванием сердца. Хроническую сердечную недостаточность? Да, несомненно. Ишемическую болезнь сердца? Да, конечно. Гипертоническую болезнь? Да. Вегетативную дизовариальную кардиомиопатию? Тоже, конечно же.
Но с другой стороны, оснований для отказа от использования антиаритмиков 1С класса у больных с любым органическим поражением сердца нет. Мы ведь не применяем препараты 1С класса, например, при постинфарктном кардиосклерозе, при остром коронарном синдроме (ОКС), при тяжелом функционально классе сердечной недостаточности.
А ведь мы тоже понимаем: если это не тяжелый функциональный класс, то у многих категорий пациентов препараты первого класса не только являются достаточно безопасными. Они нередко оказываются более эффективными, чем «Амиодарон», и лучше переносятся.
Почему мы эту проблему все-таки еще раз поднимаем? Когда мы говорим об органическом заболевании сердца, мы всегда анализируем или возвращаемся к исследованию “CAST”.
Это исследование “CAST”, которое было опубликовано в 1991-м году. Пациентам с острым (с острым, подчеркиваю) инфарктом миокарда по поводу желудочковых нарушений сердечного ритма назначались препараты 1C класса.
В 1991-м году это исследование было остановлено по причине того, что препараты 1C класса увеличили смертность по сравнению с группой плацебо. Но всегда все исследования в настоящее время пересматриваются. Сколько угодно можно говорить об этих примерах.
В 1994-1995-м году ретроспективно вернулись к этому исследованию “CAST”, еще раз проанализировали. Посмотрите, какой вывод (то, что подчеркнуто, обведено) сделали исследователи.
«Легкое» подавление желудочковой экстрасистолии препаратами “CAST” является независимым фактором риска снижения ритмической смерти на 41%.
«Легкое» подавление – это выражение самих исследователей. Если мы этой тяжелой группе пациентов назначаем небольшие дозы этих лекарственных препаратов – это привело к снижению аритмической смерти на 41%. Еще раз подчеркну: не все так хорошо, как говорится с высокой трибуны.
В настоящее время проводится под эгидой Всероссийского научного общества кардиологов исследование «ПРОСТОР». Показать эффективность и, прежде всего, безопасность применения «Пропафенона» («Пропанорма») у больных с мерцательной аритмией, которые имеют хроническую сердечную недостаточность, но фракция выброса у них сохранена.
Речь идет только о диастолической дисфункции. Мы взяли пациентов с гипертонической болезнью и с сохраненной фракцией выброса.
Почему выбран именно «Пропафенон»? Мы понимаем, что он относится к антиаритмическим препаратам 1С класса и вызывает выраженную блокаду натриевых каналов. Однако он действительно отличается от других антиаритмиков 1С класса.
Во-первых, он способствует небольшому увеличению рефрактерных периодов во всех абсолютно тканях сердца. Кроме того, у него есть умеренное бета-блокирующее действие и кальций-блокирующие свойства.
Что показало на сегодняшний день это исследование? Это исследование привело к увеличению количества пациентов, которые имеют первых функциональный класс хронической сердечной недостаточности, за счет уменьшения пациентов со вторым и третьим функциональным классом.
В этой ситуации мы понимаем, что это сделал не «Пропанорм» конкретно. Все абсолютно пациенты получали базисную медикаментозную терапию. Самое главное, что в этой ситуации «Пропанорм» не помешал динамике функционального класса ХСН.
Что касается показателей толщины задней стенки межжелудочковой перегородки. Вы видите, что действительно имело место уменьшение этих размеров, что на фоне «Пропанорма», что на фоне «Кордарона» («Cordarone»). Это не заслуга антиаритмических препаратов, а заслуга той терапии, на которой были наши пациенты.
Улучшились показатели диастолической функции левого желудочка. Очень важно, что «Пропанорм» как представитель первого С-класса не уменьшил, а даже все это способствовало увеличению фракции выброса. Что на фоне «Кордарона», что на фоне «Пропанорма».
Эффективность лекарственной терапии на фоне «Пропанорма» практически не отличалась от «Кордарона». Единственное, была такая закономерность, что через 12 месяцев эффективность снизилась. Мы пока не можем объяснить причину уменьшения этой эффективности. Либо это эффект ускользания от антиаритмического препарата, либо все-таки не такая уж стопроцентная приверженность пациентов к медикаментозной терапии.
Если у пациентов даже остались эпизоды фибрилляции предсердий, было отмечено (что на фоне «Кордарона», что на фоне «Пропанорма»), что уменьшилась длительность эпизодов на фоне проводимой терапии. А также, конечно, уменьшилась частота желудочковых сокращений во время этих эпизодов. Соответственно, это наши пациенты легче переносили, и быстрее у них купировались эпизоды фибрилляции предсердий.
Но мы обратили внимание на побочные эффекты. Это очень важный момент. Из исследования выбыли 38 больных в группе «Кордарона» и 12 в группе «Пропанорма». В этой ситуации самым грозным побочным эффектом было, конечно, удлинение интервала QT с возможностью развития двунаправленной полиморфной желудочковой тахикардии.
Таким образом, в этом исследовании «Пропанорм» пока демонстрирует лучший профиль безопасности по сравнению с «Кордароном». Частота нежелательных эффектов на фоне «Кордарона» составила 38% против 1,9% (практически 2%).
Выводы на сегодняшний день по исследованию «Простор».
Препарат первого С-класса не ухудшает показатели гемодинамики у пациентов с гипертонической болезнью и хронической сердечной недостаточностью с сохраненной систолической функцией.
Антиаритмическая эффективность «Пропанорма» через 12 месяцев составляет 48% и не уступает таковой при применении «Кордарона».
«Пропанорм» более безопасен на сегодняшний день по сравнению с «Кордароном» в отношении побочных эффектов.
Таким образом, если вами конкретно решено сохранять синусовый ритм, чем же вообще должен руководствоваться врач при выборе антиаритмического препарата. Прежде всего, мы должны взвесить переносимость лекарственного средства. А второе – это отсутствие при его применении опасных для жизни осложнений.
На сегодняшний день девиз или закон (давайте так скажем) аритмологов таков: антиаритмический препарат должен быть, в первую очередь, не столько эффективным, сколько безопасным лекарственным препаратом.
Если же все-таки вы решили не восстанавливать синусовый ритм у пациента, в принципе, на Всемирном конгрессе кардиологов эта проблема еще раз обсуждалась. Знаменитое исследование «AFFIRM».
Там антиаритмические препараты выступали против другой стратегии – стратегии «контроль ЧСС». По первичной конечной точке (а первичной конечной точкой была общая смертность) эти стратегии практически одинаковы.
Если вы все-таки решили не восстанавливать синусовый ритм, обговорили обязательно эту проблему с самим пациентом, то здесь вы можете тоже воспользоваться двумя путями подхода к контролю частоты желудочковых сокращений.
Либо держать мягкий контроль частоты желудочковых сокращений, когда во время фибрилляции предсердий частота желудочковых сокращений меньше 110-ти в одну минуту. Либо будет более жесткий контроль – ЧСС меньше 80-ти в одну минуту.
Какой же контроль выбрать. Какую стратегию применить у конкретного пациента. Все зависит от тех клинических проявлений, которые действительно вам описывает пациент.
Если он держит частоту, например, 100 в одну минуту, сохраняется, как мы говорим, все-таки тахисистолическая форма фибрилляции предсердий. Больной вам описывает клинику тех же самых проявлений сердечной недостаточности, дискомфорта – нет проблем.
Скажите пациенту, чтобы он увеличил дозу в частности бета-адреноблокаторов. В сочетании с сердечными гликозидами они сделают вашему пациенту нормосистолическую, а может быть, даже несколько наклонность к брадисистолической форме. Вы оцените по клинике, стоит ли заниматься этим жестким контролем частоты сокращений.
Еще одну проблему я хочу поднять. Нет преемственности в рекомендациях между стационаром и поликлиническим звеном.
Если в стационаре все-таки не удалось восстановить синусовый ритм, но есть все обстоятельства в пользу того, что нужно восстанавливать синусовый ритм с помощью плановой электрической кардиоверсии. Давайте дружить: стационар вместе с амбулаторным звеном.
В этой ситуации пациент должен выписаться из клиники с последующим наблюдением участкового терапевта. Должно продолжаться лечение основного заболевания. Возможно, вы будете применять помимо сердечных гликозидов, бета-блокаторов для урежения частоты желудочковых сокращений еще и антиаритмические препараты. Это ваш выбор.
Должно продолжаться антитромботическая терапия в течение трех-четырех недель до плановой электрической кардиоверсии. Мы в стационаре ждем этого пациента.
После проведения чрезпищеводной эхокардиографии, после того, как мы убедимся, что в полостях сердца нет тромбов, мы проведем электрическую кардиоверсию. А дальше определим тот план антиаритмической терапии, который мы только что с вами обсудили.
Последнее. Я хочу сказать следующее. Существуют принципы использования антиаритмических препаратов у крадиологов-аритмологов.
Первый принцип. Надо избегать назначения антиаритмиков всегда, когда это возможно. Использовать антиаритмические препараты оправдано в двух случаях.
1. При потенциально опасной для жизни аритмии. Фибрилляция предсердий не является таковой.
2. Как правило, мы антиаритмики используем по поводу второго случая: при проявлении выраженной симптоматики. Когда пациенты плохо переносят это неритмичное сердцебиение.
Второй принцип. Надо устанавливать агрессивность терапии в строгом соответствии с целью лечения. Что вы хотите получить от этого конкретного больного.
Либо избавиться от мерцательной аритмии, что невозможно. Никто не может в мире этого сделать даже при использовании хирургических методов в сочетании с антиаритмическими препаратами.
Либо просто уредить ЧСС. Сделать так, чтобы пароксизмы были реже, чтобы ЧСС во время аритмии была меньше. Это, конечно, будет оправдано.
Третий принцип. Надо соблюдать все меры, абсолютно все меры предосторожности при использовании любых антиаритмических препаратов.
Я желаю вам успеха во всем абсолютно. Самое главное – в лечение больных, которых вы лечите.